Podstawa barwienia metodą Grama, materiały, technika i zastosowania
The Barwienie metodą Grama jest najprostszą i najbardziej przydatną techniką barwienia w mikrobiologii diagnostycznej. Ta technika została stworzona przez duńskiego lekarza Hansa Christiana Grama w 1884 r., Któremu udało się sklasyfikować bakterie w Gram dodatnim i Gram ujemnym, w zależności od składu ściany komórkowej.
Technika ta została poddana pewnym modyfikacjom przez Huckera w 1921 r., Aby ustabilizować odczynniki i poprawić jakość barwnika, dzięki czemu barwienie metodą Grama jest również znane jako Gram-Hucker.
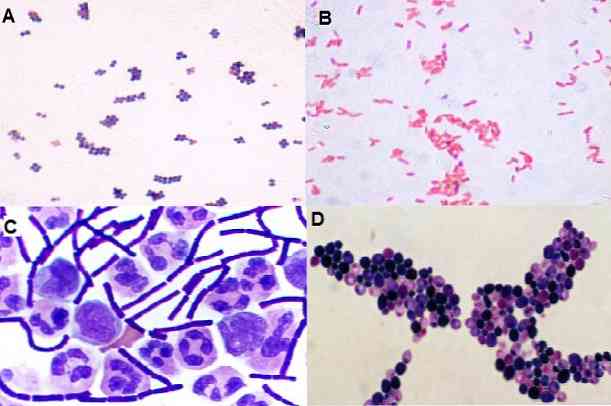
Dzięki tej technice można również obserwować formę, jaką mają mikroorganizmy, to znaczy, czy są to między innymi ziarniaki, pałeczki, coccobacilli, pleomorficzny, nitkowaty. Jak również jego rozmieszczenie w przestrzeni: w gromadzie, w łańcuchu, w izolacji, w parach, w tetradach itp..
Gdy podejrzewa się zakażenie bakteryjne, większość otrzymanych próbek powinna być rozprowadzona na szkiełku i zabarwiona za pomocą Gram do badania pod mikroskopem..
Raport Grama poprowadzi lekarza na temat tego, jaki rodzaj mikroorganizmu może być przyczyną infekcji, zanim uzyska ostateczny wynik uprawy.
W niektórych przypadkach życie pacjenta jest bardzo zagrożone, więc lekarze pilnie potrzebują raportu Grama, aby umieścić leczenie empiryczne, czekając na identyfikację mikroorganizmu.
Na przykład, jeśli Gram ujawni, że w płynie mózgowo-rdzeniowym są ziarniaki Gram-dodatnie, lekarz ustali początkową terapię antybiotykami, które eliminują ten rodzaj bakterii, zgodnie z protokołami ustalonymi dla tego leku..
Po otrzymaniu ostatecznego wyniku z nazwą wyizolowanego mikroorganizmu i jego odpowiedniego antybiogramu, lekarz oceni, czy zmienić terapię. Decyzja ta zostanie podjęta zgodnie z badaniem wrażliwości drobnoustroju na antybiotyki, które otrzymuje i ewolucją pacjenta.
Indeks
- 1 Fundacja
- 2 Materiały
- 3 Przygotowanie barwników i odczynników
- 3.1 Roztwór fioletu krystalicznego
- 3.2 Jodo-Lugol
- 3.3 Wybielanie
- 3.4 Kontrast
- 4 Przechowywanie odczynników
- 5 Przygotowanie rozprzestrzeniania się próbki do zabarwienia
- 5.1-gram bezpośrednich próbek
- 5.2-gram upraw
- 6 Technika
- 7 Narzędzie
- 8 Typowe błędy
- 9 Odniesienia
Fundacja
Jest to technika, która przedstawia 4 podstawowe kroki: barwienie, utrwalanie zaprawą, przebarwienia i kontrowanie. Dlatego też ta technika oprócz barwienia bakterii również je różnicuje.
Fiolet krystaliczny jest pierwszym używanym barwnikiem. Ma powinowactwo do peptydoglikanu, a fioletowy zabarwi wszystkie obecne bakterie, a następnie umieści się lugol, który działa jak zaprawa, czyli wywoła tworzenie nierozpuszczalnych kompleksów krystalicznego fioletu-jodu - białek rybonuklearnych wewnątrz komórki.
Bakterie Gram-dodatnie, mające grubą ściankę peptydoglikanu, tworzą więcej kompleksów (krystalicznie fioletowo-jodowy), dlatego zatrzymują barwnik.
Wpływa również na to, że ściana bakterii Gram-dodatnich zawiera większą ilość nienasyconych kwasów, które wykazują wysokie powinowactwo do środków utleniających (Lugol).
Tymczasem bakterie Gram-ujemne mają cienką warstwę peptydoglikanu, co czyni bakterie mniej skomplikowanymi niż bakterie Gram-dodatnie.
Potem następuje krok przebarwień, gdzie bakterie Gram-dodatnie i Gram-ujemne zachowują się inaczej.
Bakterie Gram-ujemne zawierają zewnętrzną błonę bogatą w lipopolisacharydy, która jest częścią jego ściany komórkowej. Tłuszcze są niszczone przez kontakt z acetonem alkoholowym, więc zewnętrzna błona ulega destabilizacji, a fioletowy kryształ jest uwalniany.
W ten sposób kontrastuje się go z safraniną lub fuksyną podstawową, przyjmując kolor czerwony.
W przypadku bakterii Gram-dodatnich są one odporne na przebarwienia, ponieważ środek bielący działa w celu zamknięcia porów, co zapobiega ucieczce kompleksu fiolet fioletu / jodu.
Dlatego zabarwienie fioletowym kryształem jest stabilne i nie ma miejsca na safraninę lub fuksynę. Z tego powodu bakterie te zabarwiają intensywnie niebieski lub fioletowy.
Materiały
Zestaw do kolorowania Gram składa się z:
- Fioletowy kryształ
- Lugol
- Alkohol acetonowy
- Safranina lub podstawowa fuksyna
Przygotowanie barwników i odczynników
Roztwór fioletu krystalicznego
Rozwiązanie A:
Fioletowy kryształ -2 gr
Alkohol etylowy 95% -20 cm3
Rozwiązanie B:
Szczawian amonowy -0,8 gr
Woda destylowana - 80 cm3
W celu ostatecznego przygotowania fioletowego kryształu roztwór 1:10 należy rozcieńczyć wodą destylowaną i zmieszać z 4 częściami roztworu B. Mieszaninę przed przechowywaniem przechowuje się przez 24 godziny. Jest filtrowany w kolbie do barwienia bursztynu za pomocą filtra papierowego.
Ilość, która będzie wykorzystywana codziennie, jest przenoszona do butelki z bursztynem z zakraplaczem.
Jodo-Lugol
Zważ i zmierz wskazaną ilość każdego związku w następujący sposób:
Kryształy Iodo - 1gr
Jodek potasu - 2gr
Woda destylowana -300 cm3
Jodek potasu rozpuszcza się stopniowo w wodzie, a następnie dodaje się jod. Roztwór jest ogolony do butelki w kolorze bursztynowym.
Ilość, która będzie wykorzystywana codziennie, jest przenoszona do mniejszej bursztynowej butelki z zakraplaczem.
Wybielanie
95% alkoholu etylowego -50 ml
Aceton - 50 ml
Jest przygotowany w równych częściach. Przykryj dobrze, ma tendencję do parowania.
Umieść w butelce z zakraplaczem.
Ten preparat zapewnia przebarwienia w umiarkowanym czasie 5-10 sekund i jest najbardziej zalecany.
Początkujący wolą używać tylko 95% alkoholu etylowego, gdzie przebarwienia są wolniejsze od 10 do 30 sekund.
Podczas gdy najbardziej doświadczeni mogą używać czystego acetonu, gdzie przebarwienia występują bardzo szybko od 1 do 5 sekund.
Kontrast
Roztwór podstawowy safraniny
Safranina -2,5 gr
Alkohol etylowy 95% -100 cm3
Po zważeniu wskazanej ilości safraniny rozpuszcza się w 100 cm3 alkoholu etylowego do 95%.
Roztwór roboczy safraniny przygotowuje się z roztworu podstawowego.
Aby to zrobić, odmierz 10 cm3 roztworu podstawowego, dodaj 90 cm3 wody destylowanej, aby uzupełnić 100 ml.
Zaleca się przeniesienie kwoty, która będzie używana codziennie, do butelki z bursztynem z zakraplaczem.
Mikroorganizmy, które wybarwiają słabo Gram-ujemne zabarwienie Gram-Hucker, takie jak niektóre beztlenowce, Legionella sp, Campylobacter sp i Brucella sp, mogą być znacznie lepiej wybarwione, jeśli zastosowana zostanie modyfikacja Barwienia Kopeloffa na Grama-Huckera, zwana barwieniem Gram-Kopeloff.
Ta technika zmienia barwnik safraniny na podstawową fuksynę. Dzięki tej modyfikacji możliwe jest skuteczne zabarwienie wyżej wymienionych mikroorganizmów.
Przechowywanie odczynników
Przygotowane barwniki należy przechowywać w temperaturze pokojowej.
Przygotowanie próbki rozprowadzone na kolor
Próbka musi zawierać co najmniej 105 mikroorganizmy przed obserwacją mikroorganizmu w rozmazie są prawdopodobne. Środki do smarowania można wytwarzać z bezpośredniej próbki lub kultur w podłożu stałym lub ciekłym.
Spready powinny być jednolite, dobrze rozmieszczone i niezbyt grube, aby uzyskać lepszą wizualizację obecnych struktur.
-Gram próbek bezpośrednich
Gram moczu bez wirówki
Mocz jest mieszany i 10 μl jest umieszczane na szkiełku. Obserwacja co najmniej jednej bakterii / pola immersyjnego wskazuje na infekcję.
Oznacza to, że kultura będzie miała w przybliżeniu ponad 100 000 CFU / ml (105 CFU / ml) moczu w 85% przypadków.
Ta metoda nie jest przydatna w przypadku liczby kolonii poniżej 100 000 CFU.
LCR Gram
Płyn mózgowo-rdzeniowy należy odwirować, usunąć supernatant i rozprowadzić osad na szkiełku. Ten płyn jest sterylny w normalnych warunkach; obserwacja bakterii wskazuje na infekcję.
Gram próbek oddechowych
Płukanie Gram, popłuczyny oskrzelowe lub oskrzelowo-pęcherzykowe, chociaż mogą występować różne mikroorganizmy, zawsze będą wskazywać na diagnozę, poza tym, że są użyteczne dla rodzaju obserwowanych komórek.
W przypadku plwociny rozmaz powinien być przygotowany z najbardziej ropnych części próbki.
Stool Gram
Nie zaleca się wykonywania Grama w tego typu próbkach, ponieważ nie ma on wartości diagnostycznej.
-Uprawy Gram
Można to zrobić na dwa sposoby, jeden z upraw płynnych, a drugi ze stałych upraw.
Płynne uprawy
Z kultur płynnych jest niezwykle prosta; pod zapalniczką pobiera się kilka pieczeni mętnego bulionu i umieszcza się je na czystym i suchym szkiełku, wykonując okrężne ruchy od środka w kierunku peryferii, aby równomiernie rozprowadzić materiał.
Pozwala się spontanicznie wyschnąć w powietrzu. Po wyschnięciu materiał jest mocowany do arkusza za pomocą ciepła. W tym celu za pomocą zacisku arkusz 3 przechodzi 4 razy przez płomień palnika Bunsena, uważając, aby nie spalić materiału.
Arkusz pozostawia się do ostygnięcia i umieszcza na mostku do kolorowania.
Solidne uprawy
Aby wykonać przedłużenie barwienia metodą Grama z kultury stałej, wykonaj następujące czynności:
Przed wyborem kolonii, które mają zostać pobrane, preparat należy przygotować, umieszczając dwie krople około sterylnego roztworu soli fizjologicznej.
Jeśli oryginalna płytka hodowlana zawiera kilka różnych typów kolonii, do wykonania Grama zostanie wybrana izolowana kolonia każdego z nich. Każda kolonia zostanie pobrana za pomocą pętli platynowej, aby rozpuścić ją w roztworze soli fizjologicznej wcześniej umieszczonym na szkiełku.
Okrągłe ruchy są przekazywane ze środka na peryferie, aby równomiernie rozłożyć kolonię na szkiełku..
Pozwala się spontanicznie wyschnąć w powietrzu. Po wyschnięciu arkusz jest mocowany ciepłem, jak wyjaśniono powyżej (płonąc suwak zapalniczką), uważając, aby nie spalić materiału.
Procedurę tę należy wykonać z każdym innym typem kolonii. Na kartce papieru należy zauważyć kolejność obserwowanych, na przykład:
Kolonia 1: Żółta kolonia beta-hemolityczna: w skupiskach obserwowano ziarniaki Gram-dodatnie
Kolonia 2: Kolonia kremu, bez hemolizy: zaobserwowano Gram-ujemne pałeczki kwasu mlekowego.
Każdy arkusz musi być oznakowany, aby wiedzieć, co obserwujemy.
Technika
Technika barwienia metodą Grama jest niezwykle prosta do wykonania i stosunkowo niedroga i nie można jej pominąć w laboratorium mikrobiologicznym.
To samo odbywa się w następujący sposób:
- Zamocuj rozmaz ciepłem i umieść na kolorowym moście.
- Arkusz jest całkowicie pokryty fioletowym szkłem przez 1 minutę.
- Umyć wodą. Nie suszyć
- Przykryj płytkę roztworem Lugola, pozostaw na 1 minutę. Umyć wodą. Nie suszyć.
- Mieszaj przez 5-10 sekund, delikatnie mieszając w alkoholu acetonowym. Lub umieść arkusz w pozycji pionowej i upuść kropelki środka odbarwiającego na powierzchnię, aż pozostałe fioletowe szkło zostanie odciągnięte. Nie przekraczaj.
- Umyć wodą. Nie suszyć.
- Wymień arkusz na kolorowy mostek i przykryj przez 30 sekund safraniną (Gram-Hucker) lub 1 minutą podstawową fuksyną (Gram-Kopeloff).
- Umyć wodą
- Pozostawić do wyschnięcia spontanicznie w pionowym powietrzu.
Po wyschnięciu umieścić 1 kroplę oleju immersyjnego, aby obserwować go pod kątem 100X w mikroskopie optycznym.
Narzędzie
Ta technika pozwala odróżnić różnice morfotypowe większości bakterii.
Drożdże wyróżniają się również tym kolorem. Biorą fiolet krystaliczny, to znaczy barwią Gram-dodatnie.
Z drugiej strony można wyróżnić bakterie Gram-dodatnie tworzące przetrwalniki, w których obserwuje się czystą przestrzeń wewnątrz prątka, gdzie powstał endospor, chociaż zarodniki nie barwią się dobrze. Aby używać zarodników, stosuje się inne techniki, takie jak Shaeffer-Fulton.
Należy zauważyć, że ta plama nie służy do barwienia wszystkich rodzajów bakterii, to znaczy istnieją przypadki, w których barwienie nie działa.
W tym przypadku można wymienić bakterie pozbawione ściany komórkowej. Na przykład: rodzaj Mycoplasma, sferoplasty, Ureaplasma, formy L i protoplasty.
Zanieczyszcza również bardzo bakterie ścianami bogatymi w kwasy mikolowe, takimi jak mykobakterie i bakterie wewnątrzkomórkowe, takie jak Chlamydias i Rickettsias.
Jest również nieefektywna w barwieniu większości bakterii krętkowych.
Istnieją bakterie tego samego rodzaju, które można zaobserwować w tej samej próbce co Gram-dodatnie i Gram-ujemne. Gdy tak się dzieje, nazywa się to zmiennym barwieniem Grama, co może wynikać ze zmiany składników odżywczych, temperatury, pH lub stężenia elektrolitów..
Częste błędy
Nadmiernie wybielać
Przesada w etapie przebarwienia może spowodować obserwację fałszywych drobnoustrojów gram-ujemnych.
Nie czekaj na wystarczająco długi czas suszenia, aby dodać olej immersyjny:
Ten błąd powoduje powstawanie miceli tłuszczowych, które utrudniają obserwację obecnych struktur. Dzieje się tak, gdy olej łączy się z cząsteczkami wody obecnymi w rozmazie.
Odwróć kolejność odczynników:
Błąd taki jak ten spowoduje, że bakterie Gram-ujemne będą wyświetlać fiolet, czyli fałszywie Gram-dodatnie.
Używaj starych upraw (stałych lub płynnych):
Może spowodować, że bakterie Gram-dodatnie zabarwią Gram-ujemne (fałszywie Gram-ujemne). Dzieje się tak, ponieważ w starych kulturach jest prawdopodobne, że istnieją martwe lub zniszczone bakterie iw tych warunkach bakterie nie zatrzymują fioletowego kryształu.
Użyj bardzo starego rozwiązania Lugola:
Z czasem lugol traci swoje właściwości, a jego kolor zanika. Jeśli używany jest już zdegenerowany odczynnik, nie będzie on dobrze utrwalał fioletu krystalicznego, dlatego istnieje możliwość uzyskania wizualizacji drobnoustrojów fałszywie Gram-ujemnych.
Niebieskawy tło
Prawidłowo odbarwione tło będzie czerwone. Niebieskie tło wskazuje, że przebarwienie było niewystarczające.
Referencje
- Ryan KJ, Ray C. 2010. Sherris. Mikrobiologia Medical, 6. wydanie McGraw-Hill, Nowy Jork, USA
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Diagnostyka mikrobiologiczna. (5 wyd.). Argentyna, redakcja Panamericana S.A..
- Forbes B, Sahm D, Weissfeld A. 2009. Diagnostyka mikrobiologiczna Bailey & Scott. 12 ed. Argentyna Panamericana S.A Editorial
- Casas-Rincón G. 1994. Ogólna mikologia. 2nd Ed Universidad Central de Venezuela, wydania biblioteczne. Wenezuela, Caracas.
- „Barwienie metodą Grama” Wikipedia, darmowa encyklopedia. 4 października 2018, 23:40 UTC. 9 grudnia 2018, 17:11. Zrobione z es.wikipedia.org.
- González M, González N. 2011. Podręcznik mikrobiologii medycznej. Druga edycja, Wenezuela: Dyrekcja mediów i publikacji Uniwersytetu Carabobo.
- López-Jácome L, Hernández-Durán M, Colín-Castro C, Ortega-Peña S, Cerón-González G, Franco-Cendejas F. Podstawowe barwienie w laboratorium mikrobiologicznym. Badania nad niepełnosprawnością. 2014; 3 (1): 10-18.


