Struktura, właściwości, nazewnictwo, zastosowanie siarczku srebra (Ag2S)
The siarczek srebra jest związkiem nieorganicznym, którego wzór chemiczny to Ag2S. Składa się z czarno-szarego ciała stałego utworzonego przez kationy Ag+ i aniony S2- w stosunku 2: 1. S2- jest bardzo podobny do Ag+, ponieważ oba są miękkimi jonami i potrafią się stabilizować.
Srebrne ozdoby mają tendencję do ciemnienia, tracąc swój charakterystyczny połysk. Zmiana koloru nie jest produktem utleniania srebra, ale jego reakcji z siarkowodorem obecnym w środowisku w niskich stężeniach; Może to wynikać z gnicia lub degradacji roślin, zwierząt lub żywności bogatej w siarkę.

H2S, którego cząsteczka zawiera atom siarki, reaguje ze srebrem według następującego równania chemicznego: 2Ag (s) + H2S (g) => Ag2S (s) + H2(g)
Dlatego Ag2S odpowiada za czarne warstwy utworzone na srebrze. Jednak w przyrodzie ta siarka występuje także w minerałach acantita i argentita. Dwa minerały różnią się od wielu innymi swoimi czarnymi i jasnymi kryształami, takimi jak kryształy na górnym obrazie.
Ag2S przedstawia struktury polimorficzne, atrakcyjne właściwości elektroniczne i optoelektroniczne, jest półprzewodnikiem i zapowiada się jako materiał do rozwoju urządzeń fotowoltaicznych, takich jak ogniwa słoneczne.
Indeks
- 1 Struktura
- 2 Właściwości
- 2.1 Masa cząsteczkowa
- 2.2 Wygląd
- 2.3 Zapach
- 2.4 Temperatura topnienia
- 2.5 Rozpuszczalność
- 2.6 Struktura
- 2.7 Współczynnik załamania światła
- 2.8 Stała dielektryczna
- 2.9 Elektronika
- 2.10 Reakcja redukcji
- 3 Nazewnictwo
- 3.1 Systematyka
- 3.2 Zapasy
- 3.3 Tradycyjne
- 4 zastosowania
- 5 referencji
Struktura
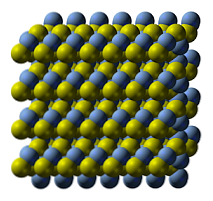
Krystaliczna struktura siarczku srebra jest przedstawiona na górnym obrazie. Niebieskie kule odpowiadają kationom Ag+, podczas gdy żółte do anionów S2-. Ag2S jest polimorficzny, co oznacza, że może przyjąć kilka układów krystalicznych w określonych warunkach temperaturowych.
Jak? Przez przejście fazowe. Jony są przestawiane w taki sposób, że wzrost temperatury i drgania ciała stałego nie zakłócają równowagi przyciągania elektrostatycznego. Gdy tak się dzieje, mówi się, że występuje przemiana fazowa, a zatem ciało stałe wykazuje nowe właściwości fizyczne (takie jak połysk i kolor).
Ag2S w normalnych temperaturach (poniżej 179ºC) ma jednoskośną strukturę krystaliczną (α- Ag2S). Poza tą fazą stałą istnieją dwa inne: bcc (sześcienny wyśrodkowany w ciele) między 179 a 586ºC, a fcc (sześcienny wyśrodkowany na ścianach) w bardzo wysokich temperaturach (δ-Ag2S).
Argentyt mineralny składa się z fazy fcc, znanej również jako β-Ag2S. Po ochłodzeniu i przekształceniu w urwisko, ich cechy strukturalne przeważają razem. Dlatego obie struktury krystaliczne współistnieją: jednoskośna i bcc. Stąd pojawiają się czarne bryły o jasnych i interesujących wydźwiękach.
Właściwości
Masa cząsteczkowa
247,80 g / mol
Wygląd
Szarawe czarne kryształy
Zapach
Toaleta.
Temperatura topnienia
836 ° C. Ta wartość zgadza się z faktem, że Ag2S jest związkiem o małym charakterze jonowym i dlatego topi się w temperaturach poniżej 1000ºC.
Rozpuszczalność
W wodzie tylko 6,21 ∙ 10-15 g / L w 25 ° C. Oznacza to, że ilość czarnej substancji stałej, która jest rozpuszczona, jest pomijalna. To znowu wynika z małego polarnego charakteru wiązania Ag-S, gdzie nie ma znaczącej różnicy elektroujemności między oboma atomami.
Również Ag2S jest nierozpuszczalny we wszystkich rozpuszczalnikach. Żadna cząsteczka nie może skutecznie oddzielić jej krystalicznych warstw w jonach Ag+ i S2- solwatowany.
Struktura
Cztery warstwy wiązań S-Ag-S można również zobaczyć na obrazie struktury, które przesuwają się nad sobą, gdy ciało stałe jest poddane zrozumieniu. To zachowanie oznacza, że mimo że jest półprzewodnikiem, jest plastyczny jak wiele metali w temperaturze pokojowej.
Warstwy S-Ag-S pasują prawidłowo ze względu na ich geometrie kątowe, które są obserwowane jako zygzak. Mając siłę zrozumienia, poruszają się po osi przemieszczenia, powodując nowe niekowalencyjne oddziaływania między atomami srebra i siarki.
Współczynnik załamania światła
2.2
Stała dielektryczna
6
Elektronika
Ag2S jest amfoterycznym półprzewodnikiem, to znaczy zachowuje się tak, jakby był typu n i tego typu str. Nie jest również kruchy, dlatego został zbadany pod kątem zastosowania w urządzeniach elektronicznych.
Reakcja redukcji
Ag2S można zredukować do srebra metalicznego przez kąpiel czarnych kawałków gorącą wodą, NaOH, aluminium i solą. Następuje następująca reakcja:
3Ag2S (s) + 2Al (s) + 3H2O (l) => 6Ag (s) + 3H2S (ac) + Al2O3(s)
Nomenklatura
Srebrny, którego konfiguracja elektroniczna to [Kr] 4d105s1, może stracić tylko jeden elektron: ten znajdujący się w najbardziej oddalonym orbicie 5s. Tak więc kation Ag+ pozostaje w konfiguracji elektronicznej [Kr] 4d10. Dlatego ma unikalną wartość +1, która określa, jak należy nazywać jej związki.
Z drugiej strony siarka ma konfigurację elektroniczną [Ne] 3s23p4, i potrzebuje dwóch elektronów do uzupełnienia oktetu walencyjnego. Kiedy otrzymuje te dwa elektrony (ze srebra), przekształca się w anion siarki, S2-, z konfiguracją [Ar]. Oznacza to, że jest izoelektroniczny do gazu szlachetnego argonu.
Więc ten Ag2S musi być wywołane zgodnie z następującą nomenklaturą:
Systematyka
Małpasiarka disrebrny Tutaj rozważamy liczbę atomów każdego elementu i są one oznaczone przedrostkami greckich liczników.
Zapasy
Siarczek srebra. W przypadku unikalnej wartościowości +1 nie jest ona określona cyframi rzymskimi w nawiasach: siarczek srebra (I); co jest nieprawidłowe.
Tradycyjny
Sulfuro argéntico. Ponieważ srebro „działa” z wartościowością +1, przyrostek -ico dodaje się do jego nazwy argentum po łacinie.
Używa
Niektóre z nowych zastosowań Ag2S to następujące:
-Zabarwienia roztworów ich nanocząstek (o różnych rozmiarach), mają działanie antybakteryjne, nie są toksyczne, a zatem mogą być stosowane w medycynie i biologii.
-Ich nanocząstki mogą tworzyć tzw. Kropki kwantowe. Pochłaniają one i emitują promieniowanie z większą intensywnością niż wiele organicznych cząsteczek fluorescencyjnych, dzięki czemu mogą zastąpić te ostatnie jako markery biologiczne.
-Struktury α-Ag2S sprawia, że wykazuje uderzające właściwości elektroniczne, które można wykorzystać jako ogniwa słoneczne. Stanowi również punkt wyjścia do syntezy nowych materiałów termoelektrycznych i czujników.
Referencje
- Mark Peplow. (17 kwietnia 2018 r.). Półprzewodnikowy siarczek srebra rozciąga się jak metal. Zrobiono z: cen.acs.org
- Współpraca: Autorzy i redaktorzy tomu III / 17E-17F-41C () Struktura krystaliczna siarczku srebra (Ag2S). W: Madelung O., Rössler U., Schulz M. (eds) Elementy niezwiązane tetrahedralnie i związki binarne I. Landolt-Börnstein - Materia skondensowana grupy III (dane numeryczne i zależności funkcjonalne w nauce i technologii), tom 41C. Springer, Berlin, Heidelberg.
- Wikipedia. (2018). Siarczek srebra. Zrobiono z: en.wikipedia.org
- Stanislav I. Sadovnikov i kol. (Lipiec 2016). Ag2S nanocząstki siarczku srebra i roztwory koloidalne: Synteza i właściwości. Zaczerpnięte z: sciencedirect.com
- Materiały Azo. (2018). Siarczek srebra (Ag2S) Półprzewodniki. Zrobiono z: azom.com
- A. Nwofe. (2015). Perspektywy i wyzwania cienkich warstw siarczku srebra: przegląd. Zakład Inżynierii Materiałowej i Energii Odnawialnej, Wydział Fizyki Przemysłowej, Ebonyi State University, Abakaliki, Nigeria.
- UMassAmherst. (2011). Wykład Demonstracje: czyszczenie zmatowionego srebra. Wykonano z: lecturedemos.chem.umass.edu
- Studiować (2018). Co to jest Siarczek srebra? - Wzór chemiczny i zastosowania. Zaczerpnięte z: study.com


