Struktura chemiczna siarczanu amonu, właściwości i zastosowania
The siarczan amonu Jest to trójskładnikowa i amoniakalna nieorganiczna sól kwasu siarkowego. Jego wzór chemiczny to (NH4)2TAK4. Dlatego proporcje stechiometryczne mówią, że dla każdego anionu siarczanowego występują dwa kationy amonowe oddziałujące z nim. Pozwala to na neutralność soli ((+1) ∙ 2 + (-2)).
Jej nomenklatura wynika z faktu, że jest to sól pochodząca z H2TAK4, zmiana przyrostka „uric” na „ato”. Zatem dwa początkowe protony są zastępowane przez NH4+, produkt reakcji z amoniakiem (NH3). Następnie równanie chemiczne dla jego syntezy wynosi: 2 NH3 + H2TAK4 => (NH4)2TAK4
Siarczan amonu jest magazynem azotu i siarki, niezbędnym w chemii gleb i nawozów.
Indeks
- 1 Struktura chemiczna
- 2 Właściwości fizyczne i chemiczne
- 2.1 Masa cząsteczkowa
- 2.2 Wygląd fizyczny
- 2.3 Zapach
- 2.4 Temperatura topnienia
- 2.5 Rozpuszczalność
- 2.6 Gęstość
- 2.7 Ciśnienie pary
- 2.8 Punkt zapłonu
- 2,9 pH
- 2.10 Stabilność
- 2.11 Rozkład
- 2.12 Korozja
- 3 zastosowania
- 3.1 W rolnictwie
- 3.2 Jako odczynnik analityczny
- 3.3 W strącaniu i izolacji białek
- 3.4 W branży
- 3.5 Inne zastosowania
- 4 odniesienia
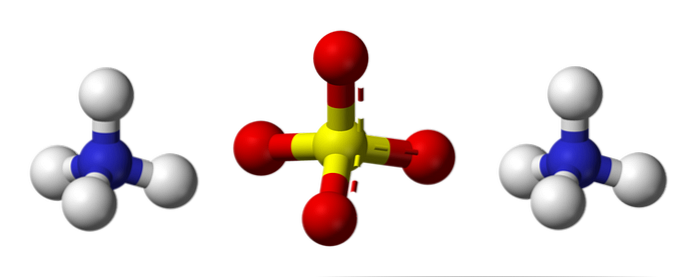
Struktura chemiczna
Górny obraz ilustruje geometrie molekularne jonów NH4+ i TAK42-. Czerwone sfery odpowiadają atomom tlenu, białe sfery odpowiadają atomom wodoru, niebieskie sfery atomowi azotu, a żółte sfery odpowiadają atomowi siarki.
Oba jony mogą być uważane za dwa czworościany, a zatem mają trzy jednostki, które oddziałują ze sobą, tworząc ortorombowy układ kryształów. Anion siarczanowy jest SO42- i jest w stanie przekazać lub przyjąć cztery wiązania wodorowe, podobnie jak kation NH4+.
Właściwości fizyczne i chemiczne
Masa cząsteczkowa
132,134 g / mol.
Wygląd fizyczny
Stałe białe. Rombowe białe lub brązowe kryształy, w zależności od poziomów zanieczyszczeń.
Zapach
Toaleta.
Temperatura topnienia
280 ° C. Ta temperatura topnienia, niska w porównaniu z innymi związkami jonowymi, wynika z faktu, że jest to sól z jednowartościowymi kationami (+1) i odmiennymi jonami w swoich rozmiarach, powodująca, że ciało stałe ma niską krystaliczną energię siatkową.
Rozpuszczalność
76,4 g / 100 g wody w temperaturze 25 ° C. To powinowactwo do wody wynika z dużej zdolności jego cząsteczek do solwatowania jonów amonowych. Z drugiej strony jest nierozpuszczalny w acetonie i alkoholu; to znaczy w rozpuszczalnikach mniej polarnych niż woda.
Gęstość
1,77 g / cm3 w 25 ° C.
Ciśnienie pary
1871 kPa w 20 ° C.
Punkt palności
26 ° C.
pH
5,0-6,0 (25 ° C, roztwór 1 M). Lekko kwaśne pH wynika z hydrolizy NH4+ w wodzie, wytwarzając H3O+ przy niskich stężeniach.
Stabilność
Stabilny w odpowiednich warunkach środowiskowych. W kontakcie z silnymi utleniaczami może się zapalić.
Rozkład
Zaczyna się rozkładać w temperaturze 150 ° C, uwalniając toksyczne opary tlenku siarki, tlenku azotu i amonu.
Korozja
Nie atakuje żelaza ani aluminium.
Używa

W rolnictwie
- Siarczan amonu jest stosowany jako nawóz w glebach alkalicznych. Sól amonowa zawiera 21% azotu i 24% siarki w swoim składzie. Istnieją jednak związki, które zapewniają większą ilość azotu niż siarczan amonu; Zaletą tego ostatniego jest wysoka koncentracja siarki.
- Siarka jest niezbędna w syntezie białek, ponieważ kilka aminokwasów, takich jak cystyna, metionina i cysteina, ma siarkę. Z tych powodów siarczan amonu jest nadal jednym z najważniejszych nawozów.
- Jest stosowany w uprawach pszenicy, kukurydzy, ryżu, bawełny, ziemniaków, konopi i drzew owocowych.
- Niskie pH gleb alkalicznych ze względu na ich udział w procesie nitryfikacji przeprowadzanej przez drobnoustroje. Stosuje się amon (NH)4+) do produkcji azotanów (NIE3-) i zwolnij H+: 2NH4+ + 4O2 => 2NO3- + 2H2O + 4H+. Wzrost stężenia wodoru obniża pH gleb alkalicznych i pozwala na większe wykorzystanie.
- Oprócz stosowania jako nawóz, siarczan amonu działa jako środek wspomagający dla rozpuszczalnych środków owadobójczych, herbicydów i fungicydów, które są rozpylane na uprawy..
- Siarczan jest zdolny do sekwestracji jonów obecnych w glebie i wodzie do nawadniania, które są niezbędne do życia niektórych patogenów. Wśród jonów, które przechwytuje siarczan amonu, są jony Ca.2+, Mg2+, wiara2+ i wiara3+. To działanie zwiększa działanie bakteriobójcze wymienionych środków.
Jako odczynnik analityczny
Siarczan amonu działa jako środek strącający w analizie elektrochemicznej, w mikrobiologicznych pożywkach hodowlanych i w przygotowaniu soli amonowych.
W precypitacji i izolacji białek
Siarczan amonu jest stosowany do izolacji i oczyszczania białek, zwłaszcza białek osocza. Do osocza dodaje się pewną ilość siarczanu amonu do pewnego stężenia; tak więc wytrąca się grupa białek.
Osad zbiera się przez odwirowanie i do supernatantu dodaje się dodatkową ilość siarczanu amonu i przy nowym stężeniu następuje wytrącanie innej grupy białek..
Powtarzanie poprzedniego procesu w postaci sekwencyjnej pozwala na uzyskanie różnych frakcji białek osocza.
Przed pojawieniem się nowych technologii biologii molekularnej procedura ta umożliwiła izolację białek osocza o dużym znaczeniu w medycynie, na przykład: immunoglobuliny, czynniki krzepnięcia itp..
W branży
Siarczan amonu działa opóźniająco na pożar w przemyśle włókienniczym. Jest stosowany jako dodatek w przemyśle galwanicznym. Jest również stosowany w produkcji nadtlenku wodoru, chlorku amonu itp..
Inne zastosowania
- Siarczan amonu jest stosowany jako środek regulujący ciśnienie osmotyczne i jako środek wytrącający sól.
- W postaci laurylosiarczanu amonu zmniejsza się napięcie powierzchniowe wody, co pozwala na oddzielenie zanieczyszczeń przez zwiększenie twardości wody.
- Jest to środek antykorozyjny.
- Jest stosowany jako dodatek do żywności, który reguluje kwasowość w cieście mącznym i chlebie.
Referencje
- OECD SIDS. (Październik 2004). Siarczan amonu. [PDF] Źródło: 27 kwietnia 2018 r. Z: inchem.org
- The Mosaic Company. (2018). Siarczan amonu. Źródło: 27 kwietnia 2018 r. Z: cropnutrition.com
- Wikipedia. (2018). Siarczan amonu. Źródło: 27 kwietnia 2018 r. Z: en.wikipedia.org
- Pubchem. (2018). Siarczan amonu. Źródło: 27 kwietnia 2018 r. Z: pubchem.ncbi.nlm.nih.gov UpSticksNGo Crew.
- (23 lipca 2015 r.). [Rysunek] Źródło: 27 kwietnia 2018 r. Z: flickr.com
- Paula Papp (22 lutego 2017). Zastosowania i zastosowania siarczanu amonu. Pobrane 27 kwietnia 2018 r. Z: business.com


