Siarczan glinu (Al2 (SO4) 3) struktura, zastosowania, rodzaje, toksyczność
The siarczan glinu jest nieorganiczną solą glinu o wzorze Al2(TAK4)3, zwykle pojawia się jako białe ciało stałe z błyszczącymi kryształami. Na kolor związku będzie miało wpływ jego stężenie żelaza i wszelkich innych zanieczyszczeń. Istnieją dwa główne rodzaje siarczanu glinu: A i B.
Na dolnym obrazie pokazano białe kryształy uwodnionego siarczanu glinu. Można zauważyć brak brązowych zabarwień, wskazujących na jony żelaza w sieci krystalicznej.

Siarczan glinu jest solą bardzo dobrze rozpuszczalną w wodzie, a w naturze rzadko można go znaleźć w postaci bezwodnej. Zazwyczaj jest uwodniony w postaci oktadecahydratu siarczanu glinu [Al2(TAK4)3.18H2O] lub heksadecydrat [Al2(TAK4)3.16H2O].
Podobnie, może tworzyć podwójne sole z potasem oraz z amonem, związkami znanymi jako ałun. Częściowo może to wynikać z powinowactwa wody w hydratach do zatrzymywania innych jonów oprócz glinu.
Siarczan glinu można rozkładać przez działanie wody w wodorotlenku glinu i kwasie siarkowym. Ta właściwość pozwoliła na wykorzystanie go jako zakwaszacza gleb.
Jest również związkiem toksycznym, zwłaszcza przez kontakt z jego proszkiem. Jednakże ma nieskończoną liczbę zastosowań i zastosowań, które wynikają z oczyszczania wody za pomocą metody koagulacji, która odbywa się poprzez jej zastosowanie w wielu gałęziach przemysłu, aż do jej zastosowania w celach terapeutycznych.
Indeks
- 1 Struktura
- 2 Co to jest (używa)
- 2.1 Koagulacja lub flokulacja wody
- 2.2 Wykorzystanie jako zaprawa farbowa i opracowanie papieru
- 2.3 Zastosowania przemysłowe
- 2.4 Zastosowania lecznicze i terapeutyczne
- 2.5 Inne zastosowania
- 3 Produkcja siarczanu glinu
- 4 typy
- 5 Toksyczność
- 6 referencji
Struktura
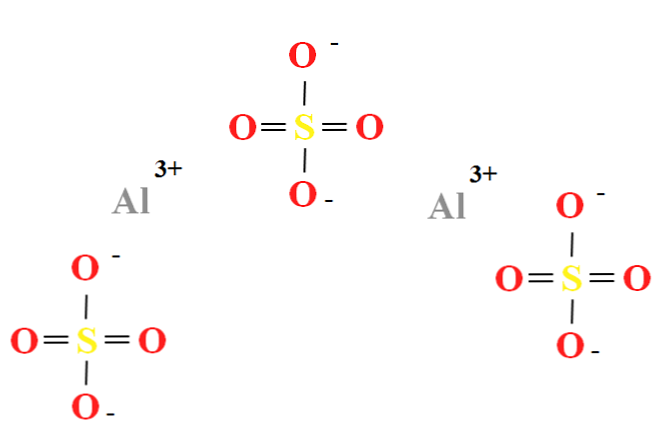
Siarczan glinu ma stosunek dwóch kationów Al3+ na każde trzy aniony SO42- (górny obraz), który można zaobserwować bezpośrednio w jego wzorze chemicznym Al2(TAK4)3.
Zauważ, że Al3+ są szarawe, podczas gdy SO42- są żółte (dla atomu siarki) i czerwone (dla atomów tlenu).
Zilustrowana struktura odpowiada bezwodnej postaci Al2(TAK4)3, ponieważ żadna cząsteczka wody nie oddziałuje z jonami. Jednak w twoich hydratach woda może być przyciągnięta do pozytywnych centrów Al3+, lub przez negatywne czworościany SO42- przez wiązania wodorowe (HOH-O-SO32-).
Al2(TAK4)3∙ 18H2Lub, na przykład, zawiera 18 cząsteczek wody w swojej stałej strukturze. Niektóre z nich mogą mieć bezpośredni kontakt z Al3+ lub z SO42-. Innymi słowy: siarczan glinu może mieć wewnętrzną lub zewnętrzną wodę koordynacyjną.
Również jego struktura może pomieścić inne kationy, takie jak Fe3+, Na+, K+, itd. Ale w tym celu konieczna jest obecność większej ilości anionów42-. Po co? Aby zneutralizować wzrost dodatnich ładunków z powodu zanieczyszczeń metalicznych.
Siarczan glinu może mieć wiele struktur, chociaż jego hydraty mają tendencję do przyjmowania jednoskośnego układu krystalicznego.
Właściwości fizyczne i chemiczne
Wygląd
Wygląda jak ciało stałe z błyszczącymi białymi kryształami, granulkami lub proszkiem.
Masa cząsteczkowa
342,31 g / mol (bezwodny).
Zapach
Jest bezwonny
Smak
Słodki smak umiarkowanie ściągający.
Temperatura topnienia
Postać bezwodna 770º C (86,5ºC w formie octadecahidratada)
Rozpuszczalność w wodzie
31,2 g / 100 ml w 0 ° C; 36,4 g / 100 ml w 20 ° C i 89 g / 100 ml w 100 ° C.
Gęstość
2,67 do 2,71 g / cm3.
Rozpuszczalność
Słabo rozpuszczalny w alkoholu etylowym.
Ciśnienie pary
Zasadniczo zero.
Stabilność
Stabilny w powietrzu.
Rozkład
Po ogrzaniu, w przybliżeniu w jego temperaturze topnienia, może ulec rozkładowi, emitując zwłaszcza tlenek siarki, toksyczny gaz.
Korozyjność
Roztwory siarczanu glinu powodują korozję aluminium. Związek może również powodować korozję metali w obecności wilgoci.
pKa
3,3 do 3,6. A jego pH wynosi 2,9 lub więcej w 5% roztworze wodnym.
Co to jest (używa)
Koagulacja lub flokulacja wody
-Po zmieszaniu z wodą (pitną, serwowaną lub odpadową) siarczan glinu powoduje wodorotlenek glinu, który tworzy kompleksy ze związkami i cząstkami w roztworze przyspieszając ich sedymentację, co przy braku obróbki siarczanem glinu wymagałoby długi czas.
-Siarczan glinu jest również stosowany do czyszczenia wody w basenie, czyniąc je bardziej atrakcyjnymi do użytku.
-Dzięki zastosowaniu siarczanu glinu uzyskuje się wodę bez zmętnienia i koloru, zwiększając jej zdolność do picia poprzez ułatwienie czyszczenia wody. Niestety ta metoda oczyszczania może prowadzić do nieznacznie zwiększonego stężenia glinu w wodzie.
-Aluminium jest bardzo toksycznym metalem, który gromadzi się w skórze, mózgu i płucach, powodując poważne zaburzenia. Ponadto nie wiadomo, jaką funkcję spełnia w żywych istotach.
-Unia Europejska wymaga, aby maksymalna dozwolona granica glinu w wodzie nie przekraczała 0,2 mg / l. Tymczasem amerykańska Agencja Ochrony Środowiska wymaga, aby maksymalny limit zanieczyszczenia wody aluminium nie przekraczał 0,05-0,2 mg / l.
-Oczyszczanie ścieków lub stosowanie siarczanu glinu pozwala na ekonomiczną eliminację lub redukcję fosforu.
Używaj jako zaprawy atramentowej i przy opracowywaniu papieru
-Siarczan glinu został użyty jako zaprawa do barwników lub atramentów, pomagając utrwalić barwiony materiał. Jego działanie naprawcze jest spowodowane przez Al (OH)3, którego galaretowata konsystencja przyczynia się do adsorpcji barwników na tekstyliach.
-Chociaż był używany od około 2000 rpne do opisanego celu, tylko barwniki organiczne wymagają zapraw. Z drugiej strony, barwniki syntetyczne nie wymagają zapraw do wypełnienia swojej funkcji.
-Został on wyparty z produkcji papieru, ale nadal jest wykorzystywany do produkcji masy papierniczej. Usuwa zanieczyszczenia, a także jest używany do wiązania materiałów, neutralizowania ładunków i kalibrowania kalafonii.
Zastosowania przemysłowe
-Jest stosowany w budownictwie w celu przyspieszenia wiązania betonu. Dodatkowo jest stosowany w hydroizolacji budynków.
-W przemyśle mydeł i tłuszczów stosuje się go do produkcji gliceryny.
-Jest on stosowany w przemyśle naftowym do produkcji katalizatorów syntetycznych, które są używane podczas pracy.
-Jest on stosowany w przemyśle farmaceutycznym jako środek ściągający w przygotowywaniu leków i kosmetyków.
-Interweniuje w produkcji barwników, takich jak karmin. Jest również stosowany jako barwnik w produkcji syntetycznych kauczuków butadienowo-styrenowych.
-W przemyśle cukrowniczym stosowany jest jako oczyszczacz melasy do trzciny cukrowej.
-Jest stosowany w produkcji dezodorantów. Dlaczego? Ponieważ powoduje zwężenie przewodów gruczołów potowych, ograniczając w ten sposób gromadzenie się potu, niezbędnego podłoża dla wzrostu bakterii powodujących nieprzyjemny zapach.
-Jest on używany w garbowaniu skóry, niezbędny do jego użycia. Dodatkowo jest stosowany do produkcji nawozów.
-Stosowany jest jako dodatek do przygotowania farb, klejów i uszczelniaczy, a także środków do czyszczenia i pielęgnacji mebli..
Zastosowania lecznicze i terapeutyczne
-Siarczan glinu jest adiuwantem immunologicznym. Dlatego spełnia funkcję przetwarzania antygenów w taki sposób, że po uwolnieniu w miejscu ich działania wytwarzają one większą produkcję przeciwciał dla zaszczepionych antygenów.
-Adiuwant Freunda i BCG, jak również inne adiuwanty, w tym te endogenne, takie jak interleukiny, są niespecyficzne dla antygenów, umożliwiając zwiększenie promienia działania immunologicznego. Umożliwiło to opracowanie szczepionek przeciwko licznym chorobom.
-Koagulacyjne działanie siarczanu glinu pozwoliło wyeliminować liczne wirusy w uzdatnionej wodzie, między innymi: Q beta, MS2, T4 i P1. Wyniki wskazują, że obróbka wody siarczanem glinu powoduje dezaktywację takich wirusów.
-Siarczan glinu stosuje się w postaci sztyftu lub proszku w leczeniu niewielkich powierzchownych ran lub otarć powstających podczas golenia.
-Jest on stosowany do produkcji octanu glinu, związku stosowanego w leczeniu niektórych schorzeń ucha. Został on również użyty, bez znaczącego sukcesu, do złagodzenia skutków ukąszeń mrówek ogniowych..
-Roztwory siarczanu glinu stosuje się w stężeniu od 5% do 10% w miejscowym leczeniu wrzodów, które umożliwiają kontrolę ich wydzielin.
-Ściągające działanie siarczanu glinu kurczy powierzchowne warstwy skóry, koagulując białka i lecząc rany.
Inne zastosowania
-Siarczan glinu pomaga w kontrolowaniu nadmiernego wzrostu glonów w stawach, jeziorach i strumieniach wody. Stosuje się go również do usuwania mięczaków, m.in. hiszpańskiego ślimaka.
-Ogrodnicy stosują ten związek do zakwaszania alkalicznych gleb. W kontakcie z jego wodą siarczan glinu rozkłada się na wodorotlenek glinu i rozcieńczony kwas siarkowy. Następnie wytrąca się wodorotlenek glinu, pozostawiając kwas siarkowy w roztworze.
-Zakwaszenie gleb spowodowane kwasem siarkowym uwidacznia się w bardzo twórczy sposób dzięki istnieniu rośliny o nazwie Hortensja, której kwiaty zmieniają kolor na niebieski w obecności kwaśnej gleby; to znaczy są wrażliwe i reagują na zmiany pH.
-Siarczan glinu bierze udział w produkcji pianki do zwalczania i kontroli ognia. Jak? Reaguje z wodorowęglanem sodu, powodując uwalnianie CO2. Ten gaz blokuje dostęp O.2 do miejsca spalania materiału; w konsekwencji rozwijało się zawieszenie broni.
Produkcja siarczanu glinu
Siarczan glinu jest syntetyzowany przez reakcję bogatego w glin związku, takiego jak ruda boksytu, z kwasem siarkowym w podwyższonych temperaturach. Następujące równanie chemiczne przedstawia reakcję:
Al2O3 + H2TAK4 -> Al2(TAK4)3 + 3 H2O
Siarczan glinu można również utworzyć w reakcji neutralizacji wodorotlenku glinu i kwasu siarkowego, zgodnie z następującą reakcją:
2 Al (OH)3 + 3 H2TAK4 + 12 H2O -> Al2(TAK4)3.18H2O
Kwas siarkowy reaguje z glinem, tworząc siarczan amonowy i uwalnianie cząsteczek wodoru w postaci gazu. Reakcja jest przedstawiona schematycznie w następujący sposób:
2 Al + 3 H2TAK4 -> Al2(TAK4)3 + 3 H2
Typy
Siarczan glinu dzieli się na dwa typy: typ A i typ B. W siarczanie glinu typu A ciała stałe są białe i mają stężenie żelaza mniejsze niż 0,5%.
W siarczanie glinu typu B ciała stałe są brązowe i mają stężenie żelaza poniżej 1,5%.
Istnieją branże produkujące siarczan glinu, które mają różne kryteria klasyfikacji. Tak więc przemysł donosi o wytwarzaniu siarczanu glinu typu A o maksymalnym stężeniu żelaza 0,1% w postaci tlenku żelazowego. Podczas gdy dla typu B wskazują maksymalne stężenie żelaza 0,35%.
Toksyczność
-Siarczan glinu jest związkiem, który wywiera toksyczne działanie w kontakcie z pyłem, powodując podrażnienie skóry, aw przypadkach częstego kontaktu zapalenie skóry.
-W oczach powoduje silne podrażnienie, nawet powodując trwałe obrażenia.
-Wdychanie powoduje podrażnienie nosa i gardła, co może powodować kaszel i wysypkę.
-Jego spożycie powoduje podrażnienie żołądka, nudności i wymioty.
-Istnieją efekty toksyczne, które chociaż nie są bezpośrednio spowodowane siarczanem glinu, są pośrednio związane z ich użyciem. Jest to przypadek pewnych toksycznych skutków glinu, spowodowanych użyciem siarczanu glinu w oczyszczaniu wody.
-Pacjenci przewlekle dializowani przy użyciu soli przygotowanych w oczyszczonej wodzie, dzięki zastosowaniu siarczanu glinu, doświadczają bardzo poważnych zaburzeń zdrowotnych. Wśród tych zaburzeń mamy niedokrwistość, otępienie przez dializę i wzrost chorób kości.
Referencje
- Wikipedia. (2018). Siarczan glinu Zrobiono z: en.wikipedia.org
- Aris Industrial Roztwór siarczanu glinu typu A i B. Pobrano z: aris.com.pe
- Christopher Boyd (9 czerwca 2014 r.). Najlepsze przemysłowe zastosowania siarczanu glinu. Zaczerpnięte z: chemservice.com
- PubChem. (2018). Bezwodny siarczan glinu. Zaczerpnięte z: pubchem.ncbi.nlm.nih.gov
- Andesia Chemicals (20 sierpnia 2009). Karta bezpieczeństwa siarczanu glinu. [PDF] Zaczerpnięte z: andesia.com
- Książka chemiczna. (2017). Siarczan glinu. Zrobiono z: chemicalbook.com


