Struktura chlorku sodu (NaCl), właściwości, zastosowania, toksyczność
The chlorek sodu, zwana również solą zwykłą lub solą stołową, jest dwuskładnikową solą nieorganiczną sodu metalu alkalicznego i chlorowca chlorowca. Jest to największy składnik soli jadalnej, a jej postać mineralna znana jest jako halit. Jego wzór cząsteczkowy to NaCl i opisuje stosunek stechiometryczny jego jonów (Na+ Cl-), a nie dyskretnej cząsteczki (Na-Cl)
Chlorek sodu jest krystalicznym białym ciałem stałym, które powstaje w wyniku połączenia sodu, srebrzystego białego metalu, który gwałtownie reaguje z wodą i pierwiastkiem chloru, trującym, korozyjnym, jasnozielonym gazem.

Na górnym obrazku pokazano część kryształów NaCl. Jak to możliwe, że dwa elementy są tak niebezpieczne jak Na i Cl2, czy może powstać sól jadalna? Po pierwsze, równanie chemiczne jego powstawania to:
2Na (s) + Cl2(g) => 2NaCl (s)
Odpowiedź leży w naturze łącza w NaCl. Będąc jonowe, właściwości Na+ i Cl- różnią się ukośnie od neutralnych atomów.
Sód jest istotnym elementem, ale w formie jonowej. Na+ jest głównym kationem zewnątrzkomórkowym o stężeniu około 140 mEq / lt i razem z towarzyszącymi mu anionami, Cl- i HCO3- (wodorowęglan), są głównie odpowiedzialne za wartość osmolarności i objętości pozakomórkowej.
Ponadto Na+ jest odpowiedzialny za generowanie i przewodzenie impulsów nerwowych w aksonach neuronów, a także inicjowanie skurczu mięśni.
NaCl jest używany od czasów starożytnych do smakowania żywności i konserwowania mięsa ze względu na jego zdolność do eliminowania bakterii i zapobiegania psuciu się.
Jest również niezbędny do produkcji wodorotlenku sodu (NaOH) i chloru molekularnego (Cl2), poprzez reakcję NaCl z wodą w wyniku hydrolizy:
2H2O (1) + 2 NaCl (s) => 2 NaOH (ac) + Cl2(g) + H2(g)
W katodzie (-) H akumuluje się2 (g) i NaOH. Tymczasem Cl gromadzi się na anodzie (+)2 (g) Wodorotlenek sodu jest stosowany w produkcji mydeł i chloru przy produkcji plastiku PVC.
Indeks
- 1 Struktura chlorku sodu
- 1.1 Jednolita komórka
- 2 Właściwości
- 2.1 Formuła molekularna
- 2.2 Masa cząsteczkowa
- 2.3 Opis fizyczny
- 2.4 Kolor
- 2.5 Smak
- 2.6 Temperatura wrzenia
- 2.7 Temperatura topnienia
- 2.8 Rozpuszczalność w wodzie
- 2.9 Rozpuszczalność w rozpuszczalnikach organicznych
- 2.10 Gęstość
- 2.11 Ciśnienie pary
- 2.12 Stabilność
- 2.13 Rozkład
- 2.14 Lepkość
- 2.15 Korozja
- 2,16 pH
- 3 zastosowania
- 3.1 W żywności
- 3.2 Zastosowania przemysłowe
- 3.3 W domu
- 3.4 Inne zastosowania
- 3.5 Zastosowania terapeutyczne
- 4 Toksyczność
- 4.1 Spożycie
- 4.2 Podrażnienie i kontakt fizyczny
- 5 referencji
Struktura chlorku sodu
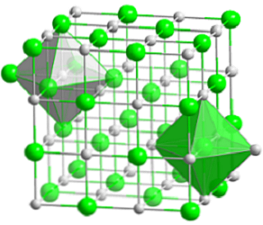
Zwarta sześcienna struktura chlorku sodu jest przedstawiona na górnym obrazie. Obszerne zielone kule odpowiadają anionom Cl-, biały, do kationów Na+. Zauważ, że kryształ NaCl składa się z sieci jonów uporządkowanych przez ich oddziaływania elektrostatyczne w stosunku 1: 1.
Chociaż słupki są pokazane na obrazie, wiązania nie są kowalencyjne, ale jonowe. Użycie pasków jest przydatne, gdy pokazuje geometrię koordynacji wokół jonu. Na przykład w przypadku NaCl każdy Na+ jest otoczony przez sześć Cl- (biały ośmiościan) i każdy Cl- sześciu Na+ (zielony ośmiościan).
Dlatego ma koordynację (6,6), której liczby wskazują, ilu sąsiadów otaczają każdy jon. Liczba po prawej wskazuje sąsiadów Na+, podczas gdy ten po lewej, Cl-.
Inne reprezentacje pomijają użycie prętów do podświetlania oktaedrycznych otworów, które posiada struktura, które wynikają z przestrzeni śródmiąższowej między sześcioma anionami Cl.- (lub kationy Na+) pakowane. Ten układ jest obserwowany w innych mono (MX) lub wieloatomowych solach nieorganicznych i jest nazywany solą gem..
Jednolita komórka
Komórka jednostkowa soli kamiennej jest sześcienna, ale które kostki dokładnie przedstawiają ją na obrazku powyżej? Ośmiościany dają odpowiedź. Oba obejmują w sumie cztery małe kostki.
Te sześciany zawierają części jonów w ich wierzchołkach, krawędziach i ścianach. Uważnie obserwuj jon Na+ znajduje się w środku i dwanaście z nich na krawędziach. Jon na jednej krawędzi może być dzielony przez cztery kostki. Są więc 4 jony Na+ (12 × 1/4 + 1 = 4).
Dla jonów Cl-, osiem znajduje się w wierzchołkach, a sześć na krawędziach. Ponieważ jony umieszczone na wierzchołkach dzielą przestrzeń z ośmioma innymi sześcianami, a na krawędziach z sześcioma mają 4 jony Cl- (8 × 1/8 + 6 × 1/2 = 4).
Poprzedni wynik jest interpretowany w następujący sposób: w komórce elementarnej NaCl występują cztery kationy Na+ i cztery aniony Cl-; proporcja zgodna ze wzorem chemicznym (Na+ dla każdego Cl-).
Właściwości
Formuła molekularna
NaCl.
Masa cząsteczkowa
58,44 g / mol.
Opis fizyczny
Krystaliczna substancja stała.
Kolor
Przezroczyste bezbarwne kryształy lub biały krystaliczny proszek.
Smak
Słony.
Temperatura wrzenia
2,575 ° F do 760 mmHg.
1465 ° C.
Temperatura topnienia
1.474 ° F (800,7 ° C).
Zarówno temperatura wrzenia, jak i temperatura topnienia odzwierciedlają ciepło niezbędne do pokonania krystalicznej energii siatkowej. Dlatego pomiary te potwierdzają charakter jonowy NaCl.
Rozpuszczalność w wodzie
Większy lub równy 100 mg / ml w 68 ° F.
36,0 g / 100 ml w 25 ° C.
Jest to w rzeczywistości higroskopijna sól, która zatrzymuje wilgoć ze środowiska.
Rozpuszczalność w rozpuszczalnikach organicznych
0,065 g / 100 ml etanolu w 25 ° C; 10 g / 100 g glicerolu w 25 ° C; 2,15 g / 100 ml ciekłego amonu w 40 ° C; 1,4 g / 100 ml metanolu w 25 ° C; 7,15 g / 100 glikolu etylenowego w 25 ° C i 5,21 g / 100 g kwasu mrówkowego w 25 ° C.
Gęstość
2,165 g / cm3 w 77 ° C.
Ciśnienie pary
1 mmHg do 1589 ° F.
Stabilność
Jest stabilny w zalecanych warunkach przechowywania.
Rozkład
Po podgrzaniu do wysokiej temperatury rozkłada się wydzielając pary kwasu chlorowodorowego i tlenku disodu.
Lepkość
Lepkość roztworów nasyconych 1,93 mPa-s.
Korozja
Działa korozyjnie na wiele metali.
pH
6,7 do 7,3 w roztworze wodnym.
Używa
W jedzeniu
-Chlorek sodu jest używany od czasów starożytnych w celu poprawy smaku żywności i jej konserwacji. Solenie mięsa jest sposobem na zachowanie go przed działaniem bakterii, ponieważ opóźnia rozkład białka.
-Z drugiej strony, sól zwiększa osmolarność wokół mięsa, co powoduje absorpcję przez osmozę wody bakterii powodując jej eliminację.
Zastosowania przemysłowe
Przemysł spożywczy
-W przemyśle spożywczym sól stosuje się jako wzmacniacz smaku, dodatek do kontroli fermentacji, środek do kontroli tekstury i wywoływacz koloru. Na przykład dodaje się sól w celu podkreślenia koloru bekonu, szynki i innych produktów mięsnych.
-Sól służy jako środek wiążący w produkcji kiełbas. Przyczynia się do tworzenia żelu wiążącego złożonego z mięsa, tłuszczu i wilgoci.
-Podczas przetwarzania mąki do wypieku chleba dodaje się sól podczas gotowania w celu kontrolowania szybkości fermentacji ciasta chlebowego. Służy również do wzmacniania glutenu i jako wzmacniacz smaku, a także do wypełniania wypieków.
-Stosuje się go do produkcji płatków śniadaniowych, mieszanych lub przygotowanych mąk, frytek, posiłków dla psów i kotów itp..
Synteza produktów chemicznych
-Chlorek sodu jest stosowany jako surowiec do produkcji wodorotlenku sodu i chloru, który z kolei jest przydatny w wielu gałęziach przemysłu chemicznego.
-Sól jest używana do przetwarzania różnych metali, na przykład aluminium, miedzi, stali i wanadu. Jest także używany do wytwarzania chloranu sodu, który jest następnie wykorzystywany w syntezie dwutlenku chloru, wybielacza na bazie tlenu. Dwutlenek chloru jest mniej szkodliwy dla środowiska niż inne wybielacze.
W przemyśle skórzanym
-Sól jest używana do hamowania działania bakterii w skórze, a także do pomocy w jej ponownym nawodnieniu.
W przemyśle włókienniczym
-Sól jest używana jako zaprawa do barwienia tkanin. Jest on używany jako płukanka solanki w celu usunięcia zanieczyszczeń organicznych i stworzenia dodatniego ładunku na powierzchni tkanin, który umożliwia połączenie ujemnie naładowanych barwników.
W przemyśle naftowym
-W poszukiwaniach ropy i gazu sól jest ważnym składnikiem płynów wiertniczych. Służy do flokulacji i zwiększenia gęstości płynów wiertniczych, co pozwala przezwyciężyć wysokie ciśnienie gazu w dołkach, które mają zostać osiągnięte. Ponadto sól utrzymuje nasycenie cieczy wiertniczej.
-Sól pomaga zagęścić glebę, na której budowane są drogi. Zmniejsza przemieszczenie spowodowane w podłożu przez zmiany wilgotności i ruchu samochodowego.
W domu
Sól została użyta przez wcieranie w czyszczenie powierzchni, garnków i patelni. Również w zapobieganiu pleśni i jako odplamiacz. Jest również stosowany w wielu markach szamponów i past do zębów.
Inne zastosowania
Na drogach
-W oczekiwaniu na opady śniegu drogi są pokryte solanką, co zapobiega związaniu lodu z powierzchnią drogi. Do rozmrażania stosuje się mieszaninę solanki i soli i czasami dodaje się inne składniki chemiczne, takie jak chlorki magnezu lub wapnia. Stosowanie soli i solanki nie jest skuteczne w temperaturach poniżej -10 ° C.
Przy dodawaniu soli następuje spadek punktu krioskopowego, właściwości koligatywnej roztworów, co w pewien sposób utrudnia tworzenie się lodu.
-Ze względu na stan higroskopijny sól jest stosowana jako tani środek osuszający.
W żywicach używanych do zmiękczania wody
Twarda woda zawiera jony wapnia i magnezu, które utrudniają działanie mydła i wytwarzają osady materiałów alkalicznych w różnych urządzeniach i rurach. W zmiękczaniu wody stosuje się żywice jonowymienne. Sól służy do przygotowania i regeneracji żywic.
Na gaśnicach
Chlorek sodu jest stosowany w gaśnicach do zwalczania pożarów, w których obecne są palne metale, takie jak stopy magnezu, potasu, sodu i NK.
Sól działa jak radiator, a także jako kruszarka, która ogranicza dostęp tlenu do ognia.
W okularach
Kryształy chlorku sodu stosuje się w elementach optycznych, takich jak okna i pryzmaty, zwłaszcza do światła podczerwonego. Jednakże, ponieważ sól jest bardzo higroskopijna, występuje rodzaj mrozu pokrywającego soczewki. Z tego powodu soczewki chlorku sodu zostały zastąpione soczewkami selenku cynku (ZnSe).
Zastosowania terapeutyczne
Aby uzupełnić brak soli w organizmie
-Kiedy dochodzi do wyczerpania ciała Na+, należy wymienić, aby utrzymać osmolarność zewnątrzkomórkową, przewodnictwo nerwowe i skurcz mięśni.
-NaCl stosuje się w leczeniu i zapobieganiu niedoborom sodu i chloru, wynikającym z nadmiernej potliwości podczas ekspozycji na wysokie temperatury. Jest również stosowany w nadmiernej diurezie lub nadmiernym ograniczaniu spożycia soli.
-Podawanie pozajelitowe roztworu 045% NaCl stosuje się w leczeniu cukrzycy hiperosmolarnej. Pełni funkcję rehydracyjną i służy do oceny stanu czynności nerek.
-Iniekcje roztworów hipertonicznych o stężeniu NaCl większym niż 0,9% w / v,
-Są one używane, gdy występuje poważne wyczerpanie Na+, przywrócenie zasadniczego jonu. Ta hiponatremia może być konsekwencją leczenia wolnymi elektrolitami lub stężeniem Na+.
Hiponatremia może być również spowodowana nadmiernym spożyciem wody, nie kontrolowanym przez nieodpowiednią czynność nerek.
W zabiegach i niekonwencjonalnych zastosowaniach
-Roztwory do inhalacji NaCl stosuje się do rozcieńczania leków stosowanych w procesie nebulizacji. Jest również stosowany do mycia i nawadniania tchawicy. 0,9% roztwór soli w aerozolu do nosa.
-20% roztwory NaCl stosuje się do wewnątrzbłonowej instalacji przezbrzusznej, co powoduje późną aborcję w drugim trymestrze ciąży.
-Chlorek sodu może być stosowany jako miejscowy środek antyseptyczny. Dzięki swojej zdolności osmotycznej jest w stanie odwodnić szerokie spektrum wirusów i bakterii w stanie niespalonym; dlatego jest stosowany jako bolesny środek antyseptyczny do dezynfekcji ran.
Toksyczność
Spożycie
Ma to szkodliwy wpływ na zdrowie tylko wtedy, gdy spożycie jest wysokie i przez długi czas. W tych okolicznościach wystąpiłaby hipernatremia, co spowodowałoby wzrost objętości pozakomórkowej, prowadzący do wysokiego ciśnienia krwi.
Podrażnienie i kontakt fizyczny
Działa toksycznie tylko wtedy, gdy inhalacja jest bardzo wysoka. W kontakcie ze skórą w nadmiernej formie może spowodować jej suchość. Wreszcie powoduje chwilowe podrażnienie po kontakcie z oczami.
Referencje
- Shiver i Atkins. (2008). Chemia nieorganiczna (Wydanie czwarte, strony 84, 90, 93, 263). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. Chemia (8 wyd.). CENGAGE Learning, str. 482-483.
- Chlorek sodu (2018). Chlorek sodu: korzyści, zastosowania, właściwości, zagrożenia. Zrobiono z: clorurodesodio.org
- PubChem. (2018). Chlorek sodu. Źródło: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Chlorek sodu. Zrobiono z: en.wikipedia.org
- Elementy amerykańskie. (2018). Chlorek sodu. Zrobiono z: americanelements.com


