Struktura kwasu bromowodorowego (HBr), właściwości, tworzenie, zastosowania
The Kwas bromowodorowy jest związkiem nieorganicznym, który powstaje z wodnego roztworu gazu zwanego bromkiem wodoru. Jego wzór chemiczny to HBr i można go traktować w różny sposób: jako wodorek cząsteczkowy lub halogenowodór w wodzie; to znaczy hydrazyd.
W równaniach chemicznych należy zapisać jako HBr (ac), aby wskazać, że jest to kwas bromowodorowy, a nie gaz. Ten kwas jest jednym z najsilniejszych znanych, nawet bardziej niż kwas solny, HCl. Wyjaśnienie tego leży w naturze jego wiązania kowalencyjnego.
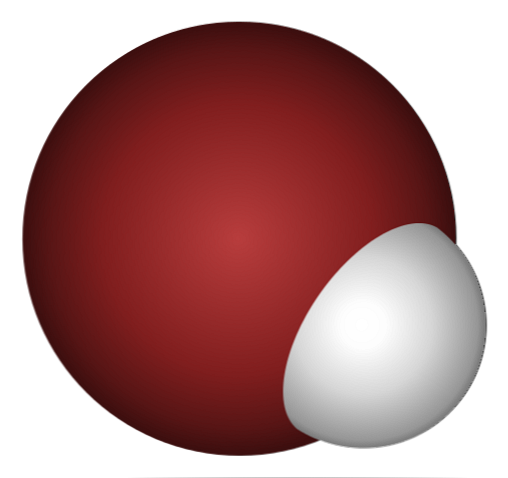
Dlaczego HBr taki kwas, a jeszcze bardziej rozpuszczony w wodzie? Ponieważ wiązanie kowalencyjne H-Br jest bardzo słabe, z powodu słabego nakładania się orbitali 1s H i 4p Br.
Nie jest to zaskakujące, jeśli przyjrzysz się uważnie powyższemu obrazowi, gdzie wyraźnie atom bromu (brązowy) jest znacznie większy niż atom wodoru (biały).
W konsekwencji każde zakłócenie powoduje rozpad wiązania H-Br, uwalniając jon H+. Następnie kwas bromowodorowy jest kwasem Brönsteda, ponieważ przenosi protony lub jony wodorowe. Jego siła jest taka, że stosuje się go w syntezie kilku związków organobromowanych (takich jak 1-bromoetan, CH3CH2Br).
Kwas bromowodorowy jest, po wodzie, HI, jednym z najsilniejszych i najbardziej użytecznych hydrocydów do trawienia niektórych stałych próbek.
Indeks
- 1 Struktura kwasu bromowodorowego
- 1.1 Kwasowość
- 2 Właściwości fizyczne i chemiczne
- 2.1 Formuła molekularna
- 2.2 Masa cząsteczkowa
- 2.3 Wygląd fizyczny
- 2.4 Zapach
- 2.5 Próg zapachu
- 2.6 Gęstość
- 2.7 Temperatura topnienia
- 2.8 Temperatura wrzenia
- 2.9 Rozpuszczalność w wodzie
- 2.10 Gęstość pary
- 2,11 pKa kwasowości
- 2.12 Pojemność kaloryczna
- 2.13 Standardowa entalpia molowa
- 2.14 Standardowa entropia molowa
- 2.15 Temperatura zapłonu
- 3 Nazewnictwo
- 4 Jak powstaje?
- 4.1 Mieszanina wodoru i bromu w wodzie
- 4.2 Tribromek fosforu
- 4.3 Dwutlenek siarki i brom
- 5 zastosowań
- 5.1 Przygotowanie bromków
- 5.2 Synteza halogenków alkilowych
- 5.3 Katalizator
- 6 referencji
Struktura kwasu bromowodorowego
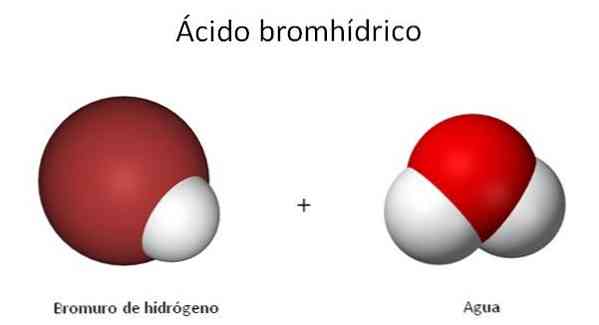
Struktura H-Br jest pokazana na obrazie, którego właściwości i właściwości, nawet gazu, są ściśle związane z jego roztworami wodnymi. Dlatego przychodzi moment, w którym dochodzi do zamieszania co do tego, który z dwóch związków jest nawiązany do: HBr lub HBr (ac).
Struktura HBr (ac) różni się od struktury HBr, ponieważ teraz cząsteczki wody solwatują tę cząsteczkę dwuatomową. Gdy jest wystarczająco blisko, H jest przenoszone+ do cząsteczki H2Lub jak wskazano w następującym równaniu chemicznym:
HBr + H2O => Br-- + H3O+
Zatem struktura kwasu bromowodorowego składa się z jonów Br-- i H3O+ oddziaływanie elektrostatyczne. Teraz jest trochę inaczej niż wiązanie kowalencyjne H-Br.
Jego duża kwasowość jest spowodowana masywnym anionem Br- ledwo wchodzi w interakcję z H3O+, nie mógł powstrzymać go przed przeniesieniem H+ do innego otaczającego gatunku chemicznego.
Kwasowość
Na przykład Cl- i F- chociaż nie tworzą wiązań kowalencyjnych z H3O+, mogą oddziaływać poprzez inne siły międzycząsteczkowe, takie jak mostki wodorowe (które tylko F- jest w stanie je zaakceptować). Most wodorowy F--H-OH2+ „Utrudnij” darowiznę H+.
Z tego powodu kwas fluorowodorowy, HF, jest słabszym kwasem w wodzie niż kwas bromowodorowy; ponieważ oddziaływania jonowe Br- H3O+ nie przejmuj się przenoszeniem H+.
Jednakże, chociaż woda jest obecna w HBr (ac), jej zachowanie na końcu rachunku jest podobne do zachowania cząsteczki H-Br; to jest H+ Przenosi się go z HBr lub Br-H3O+.
Właściwości fizyczne i chemiczne
Formuła molekularna
HBr.
Masa cząsteczkowa
80,972 g / mol. Należy zauważyć, że, jak wspomniano w poprzedniej części, rozważany jest tylko HBr, a nie cząsteczka wody. Jeśli masa cząsteczkowa pochodzi ze wzoru Br-H3O+ miałaby wartość około 99 g / mol.
Wygląd fizyczny
Bezbarwna lub jasnożółta ciecz, która zależy od stężenia rozpuszczonego HBr. Im bardziej jest żółta, tym bardziej będzie skoncentrowana i niebezpieczna.
Zapach
Ostry, irytujący.
Próg zapachu
6,67 mg / m3.
Gęstość
1,49 g / cm3 (roztwór wodny w 48% w / w). Ta wartość, podobnie jak odpowiadająca temperaturom topnienia i wrzenia, zależy od ilości rozpuszczonego HBr w wodzie.
Temperatura topnienia
-11ºC (12ºF, 393ºK) (roztwór wodny o stężeniu 49% w / w).
Temperatura wrzenia
122 ° C (252 ° F 393 ° K) przy 700 mm Hg (roztwór wodny 47-49% w / w).
Rozpuszczalność w wodzie
-221 g / 100 ml (w 0 ° C).
-204 g / 100 ml (15 ° C).
-130 g / 100 ml (100 ° C).
Te wartości odnoszą się do gazowego HBr, a nie do kwasu bromowodorowego. Jak można zauważyć, zwiększenie temperatury zmniejsza rozpuszczalność HBr; zachowanie, które jest naturalne w gazach. W konsekwencji, jeśli wymagane są stężone roztwory HBr (ac), lepiej jest z nimi pracować w niskich temperaturach.
W przypadku pracy w wysokich temperaturach HBr ucieknie w postaci gazowych cząsteczek dwuatomowych, więc reaktor musi zostać uszczelniony, aby zapobiec wyciekowi.
Gęstość pary
2,71 (w odniesieniu do powietrza = 1).
Kwasowość pKa
-9,0. Ta stała tak negatywna wskazuje na jej wielką siłę kwasowości.
Pojemność kaloryczna
29,1 kJ / mol.
Standardowa entalpia molowa
198,7 kJ / mol (298 ºK).
Standardowa entropia molowa
-36,3 kJ / mol.
Punkt zapłonu
Niepalny.
Nomenklatura
Jego nazwa „kwas bromowodorowy” łączy dwa fakty: obecność wody, a brom ma wartość -1 w związku. W języku angielskim jest to nieco bardziej oczywiste: kwas bromowodorowy, gdzie przedrostek „hydro” (lub hydro) odnosi się do wody; chociaż, naprawdę, może również odnosić się do wodoru.
Brom ma wartość -1, ponieważ jest związany z atomem wodoru mniej elektroujemny niż jest; ale jeśli jest połączony lub oddziałuje z atomami tlenu, może mieć wiele wartościowości, takich jak: +2, +3, +5 i +7. Z H może przyjąć tylko jedną wartościowość i dlatego przyrostek -ico dodaje się do jego nazwy.
Podczas gdy HBr (g), bromowodór, jest bezwodny; to znaczy, że nie ma wody. Dlatego jest nazywany zgodnie z innymi standardami nomenklatury, odpowiadającymi standardom halogenków wodoru.
Jak się tworzy?
Istnieje kilka metod syntezy kwasu bromowodorowego. Niektóre z nich to:
Mieszanina wodoru i bromu w wodzie
Bez opisywania szczegółów technicznych kwas ten można otrzymać z bezpośredniej mieszaniny wodoru i bromu w reaktorze wypełnionym wodą.
H2 + Br2 => HBr
W ten sposób, gdy tworzy się HBr, rozpuszcza się w wodzie; Może to przeciągnąć go do destylacji, więc roztwory mogą być ekstrahowane przy różnych stężeniach. Wodór jest gazem, a brom ciemnoczerwonym płynem.
Tribromek fosforu
W bardziej skomplikowanym procesie miesza się piasek, uwodniony czerwony fosfor i brom. Pułapki wodne umieszcza się w łaźniach lodowych, aby zapobiec ucieczce HBr i utworzeniu zamiast tego kwasu bromowodorowego. Reakcje są:
2P + 3Br2 => 2PBr3
PBr3 + 3H2O => 3HBr + H3PO3
Dwutlenek siarki i brom
Innym sposobem przygotowania jest reakcja bromu z dwutlenkiem siarki w wodzie:
Br2 + TAK2 + 2H2O => 2HBr + H2TAK4
To jest reakcja redoks. Fr.2 zmniejsza, zyskuje elektrony, łącząc się z wodorami; podczas gdy SO2 utlenia się, traci elektrony, gdy tworzy więcej wiązań kowalencyjnych z innymi tlenami, jak w kwasie siarkowym.
Używa
Przygotowanie bromków
Sole bromkowe można wytworzyć, jeśli HBr (ac) poddaje się reakcji z wodorotlenkiem metalu. Na przykład rozważa się produkcję bromku wapnia:
Ca (OH)2 + 2HBr => CaBr2 + H2O
Innym przykładem jest bromek sodu:
NaOH + HBr => NaBr + H2O
W ten sposób można przygotować wiele nieorganicznych bromków.
Synteza halogenków alkilowych
A co z organicznymi bromkami? Są to związki boroorganiczne: RBr lub ArBr.
Odwodnienie alkoholi
Surowcem do ich uzyskania mogą być alkohole. Gdy są sprotonowane przez kwasowość HBr, tworzą wodę, która jest dobrą grupą wychodzącą, a zamiast tego zostaje włączony objętościowy atom Br, który stanie się kowalencyjnie związany z węglem:
ROH + HBr => RBr + H2O
To odwodnienie przeprowadza się w temperaturach powyżej 100 ° C, w celu ułatwienia zerwania wiązania R-OH2+.
Dodatek do alkenów i alkinów
Cząsteczka HBr może być dodana z jej wodnego roztworu do podwójnego lub potrójnego wiązania alkenu lub alkinu:
R2C = CR2 + HBr => RHC-CRBr
RC≡CR + HBr => RHC = CRBr
Można uzyskać kilka produktów, ale w prostych warunkach produkt najpierw tworzy się, gdy brom jest połączony z węglem wtórnym, trzeciorzędowym lub czwartorzędowym (zasada Markovnikova).
Te halogenki wpływają na syntezę innych związków organicznych, a ich zakres zastosowań jest bardzo szeroki. Ponadto niektóre z nich można nawet wykorzystać w syntezie lub projektowaniu nowych leków.
Eteryczne kliknięcie
Z eterów można otrzymać jednocześnie dwa halogenki alkilowe, z których każdy zawiera jeden z dwóch łańcuchów bocznych R lub R 'początkowego eteru R-O-R'. Zdarza się coś podobnego do odwodnienia alkoholi, ale jego mechanizm reakcji jest inny.
Reakcję można schematować za pomocą następującego równania chemicznego:
ROR '+ 2HBr => RBr + R'Br
A woda jest również uwalniana.
Katalizator
Jego kwasowość jest taka, że można go stosować jako skuteczny katalizator kwasowy. Zamiast dodawać anion Br- do struktury molekularnej otwiera drogę dla innej cząsteczki.
Referencje
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chemia organiczna. Aminy (10th wydanie.). Wiley Plus.
- Carey F. (2008). Chemia organiczna (Szósta edycja). Mc Graw Hill.
- Steven A. Hardinger. (2017). Ilustrowany słownik chemii organicznej: kwas bromowodorowy. Źródło: chem.ucla.edu
- Wikipedia. (2018). Kwas bromowodorowy. Źródło: en.wikipedia.org
- PubChem. (2018). Kwas bromowodorowy. Źródło: pubchem.ncbi.nlm.nih.gov
- Narodowy Instytut Bezpieczeństwa i Higieny Pracy. (2011). Bromowodór [PDF] Źródło: insht.es
- PrepChem. (2016). Wytwarzanie kwasu bromowodorowego. Źródło: prepchem.com


