Właściwości bezwodne, sposób ich tworzenia, nazewnictwo, zastosowania
The bezwodniki są to związki chemiczne, które powstają w wyniku połączenia dwóch cząsteczek poprzez uwolnienie wody. Tak więc może to być postrzegane jako odwodnienie początkowych substancji; chociaż nie jest to dokładnie prawda.
W chemii organicznej i nieorganicznej wspomina się o nich, a w obu gałęziach ich rozumienie różni się w znacznym stopniu. Na przykład w chemii nieorganicznej tlenki zasadowe i kwasowe są uważane za bezwodniki ich wodorotlenków i kwasów odpowiednio, ponieważ te pierwsze reagują z wodą tworząc ten ostatni..

Tutaj może powstać zamieszanie między określeniami „bezwodny” i „bezwodnik”. Ogólnie, bezwodny odnosi się do związku, który został odwodniony bez zmian w jego chemicznym charakterze (brak reakcji); podczas gdy w przypadku bezwodnika zachodzi zmiana chemiczna, odzwierciedlona w strukturze molekularnej.
Jeśli wodorotlenki i kwasy zostaną porównane z odpowiadającymi im tlenkami (lub bezwodnikami), zaobserwuje się reakcję. W przeciwieństwie do tego, niektóre tlenki lub sole mogą być uwodnione, tracą wodę i pozostają tymi samymi związkami; ale bez wody, to znaczy bezwodnej.
Natomiast w chemii organicznej przez bezwodnik rozumie się początkową definicję. Na przykład, jednym z najbardziej znanych bezwodników są pochodne kwasów karboksylowych (górny obraz). Składają się one z połączenia dwóch grup acylowych (-RCO) za pomocą atomu tlenu.
W swojej ogólnej strukturze wskazano R1 dla grupy acylowej i R2 dla drugiej grupy acylowej. Ponieważ R1 i R2 są różne, pochodzą z różnych kwasów karboksylowych, a następnie są asymetrycznym bezwodnikiem kwasowym. Gdy oba podstawniki R (niezależnie od tego, czy są aromatyczne) są takie same, mówimy w tym przypadku o symetrycznym bezwodniku kwasowym.
W momencie łączenia dwóch kwasów karboksylowych w celu utworzenia bezwodnika, woda może być utworzona lub nie, jak również inne związki. Wszystko będzie zależało od struktury tych kwasów.
Indeks
- 1 Właściwości bezwodników
- 1.1 Reakcje chemiczne
- 2 Jak powstają bezwodniki?
- 2.1 Cykliczne bezwodniki
- 3 Nazewnictwo
- 4 Aplikacje
- 4.1 Bezwodniki organiczne
- 5 Przykłady
- 5.1 Bezwodnik bursztynowy
- 5.2 Bezwodnik glutarowy
- 6 referencji
Właściwości bezwodników
Właściwości bezwodników będą zależeć od tego, do czego się odnosisz. Prawie wszystkie mają wspólną cechę, że reagują z wodą. Jednak dla tak zwanych bezwodników zasadowych w nieorganicznych, w rzeczywistości kilka z nich jest nawet nierozpuszczalnych w wodzie (MgO), więc to stwierdzenie skupi się na bezwodnikach kwasów karboksylowych.
Temperatura topnienia i wrzenia spada na strukturę molekularną i oddziaływania międzycząsteczkowe dla (RCO)2Albo jest to ogólny wzór chemiczny tych związków organicznych.
Jeśli masa cząsteczkowa (RCO)2Lub jest niski, prawdopodobnie jest to bezbarwna ciecz w temperaturze pokojowej i ciśnieniu. Na przykład bezwodnik octowy (lub bezwodnik etanowy), (CH3CO)2Lub jest to ciecz o większym znaczeniu przemysłowym, która jest bardzo rozległa.
Reakcję między bezwodnikiem octowym i wodą reprezentuje następujące równanie chemiczne:
(CH3CO)2O + H2O => 2CH3COOH
Zauważ, że po dodaniu cząsteczki wody uwalniane są dwie cząsteczki kwasu octowego. Odwrotna reakcja nie może jednak wystąpić w przypadku kwasu octowego:
2CH3COOH => (CH3CO)2O + H2O (tak się nie dzieje)
Konieczne jest skorzystanie z innej trasy syntetycznej. Z drugiej strony kwasy dikarboksylowe mogą to zrobić przez ogrzewanie; ale zostanie to wyjaśnione w następnej sekcji.
Reakcje chemiczne
Hydroliza
Jedną z najprostszych reakcji bezwodników jest ich hydroliza, którą właśnie wykazano dla bezwodnika octowego. Oprócz tego przykładu mamy bezwodnik kwasu siarkowego:
H2S2O7 + H2O <=> 2H2TAK4
Tutaj masz nieorganiczny bezwodnik kwasowy. Zauważ, że dla H2S2O7 (zwany również kwasem disiarczkowym), sama reakcja jest odwracalna, więc ogrzewanie H2TAK4 Koncentrat powoduje tworzenie się jego bezwodnika. Jeśli natomiast jest to rozcieńczony roztwór H2TAK4, SO jest uwalniane3, bezwodnik siarkowy.
Estryfikacja
Bezwodniki kwasowe reagują z alkoholami, z pirydyną w ośrodku, otrzymując ester i kwas karboksylowy. Na przykład rozważa się reakcję między bezwodnikiem octowym a etanolem:
(CH3CO)2O + CH3CH2OH => CH3CO2CH2CH3 + CH3COOH
Tworząc etanolan estru etylowego, CH3CO2CH2CH3, i kwas etanowy (kwas octowy).
Praktycznie to, co się dzieje, to zastąpienie wodoru grupy hydroksylowej grupą acylową:
R1-OH => R1-OCOR2
W przypadku (CH3CO)2Albo twoja grupa acylowa to COCH3. Dlatego mówi się, że grupa OH cierpi na acylację. Jednak acylowanie i estryfikacja nie są wymiennymi koncepcjami; Acylacja może zachodzić bezpośrednio w pierścieniu aromatycznym, znanym jako acylowanie Friedela-Craftsa.
Tak więc alkohole w obecności bezwodników kwasowych są estryfikowane przez acylowanie.
Z drugiej strony, tylko jedna z dwóch grup acylowych reaguje z alkoholem, druga pozostaje z wodorem tworząc kwas karboksylowy; w przypadku (CH3CO)2Lub jest to kwas etanowy.
Amidacja
Bezwodniki kwasowe reagują z amoniakiem lub z aminami (pierwszorzędowymi i drugorzędowymi) dając amidy. Reakcja jest bardzo podobna do opisanej właśnie estryfikacji, ale ROH zastępuje się aminą; na przykład drugorzędowa amina, R2NH.
Ponownie reakcja pomiędzy (CH3CO)2O i dietyloamina, Et2NH:
(CH3CO)2O + 2Et2NH => CH3CONEt2 + CH3COO-+NH2Et2
Tworzą się dietyloacetamid, CH3CONEt2, i karboksylowa sól amoniowa, CH3COO-+NH2Et2.
Chociaż równanie może wydawać się trochę trudne do zrozumienia, wystarczy obserwować, jak grupa -COCH3 zastąp H w Et2NH tworzy amid:
Et2NH => Et2NCOCH3
Bardziej niż amidacja, reakcja jest nadal acylacją. Wszystko jest streszczone w tym słowie; tym razem amina cierpi na acylację, a nie na alkohol.
Jak powstają bezwodniki?
Nieorganiczne bezwodniki powstają w wyniku reakcji pierwiastka z tlenem. Zatem, jeśli pierwiastek jest metaliczny, powstaje zasadowy tlenek lub bezwodnik metalu; a jeśli jest niemetalowa, powstaje tlenek niemetaliczny lub bezwodnik kwasowy.
W przypadku bezwodników organicznych reakcja jest inna. Dwa kwasy karboksylowe nie mogą wiązać się bezpośrednio do uwalniania wody i tworzyć bezwodnik kwasowy; wymagany jest udział związku, który nie został jeszcze wymieniony: chlorek acylu, RCOCl.
Kwas karboksylowy reaguje z chlorkiem acylu, wytwarzając odpowiedni bezwodnik i chlorowodór:
R1COCl + R2COOH => (R1CO) O (COR2) + HCl
CH3COCl + CH3COOH => (CH3CO)2O + HCl
CH3 pochodzi z grupy acetylowej, CH3CO-, a drugi jest już obecny w kwasie octowym. Wybór konkretnego chlorku acylu, jak również kwasu karboksylowego, może spowodować syntezę symetrycznego lub asymetrycznego bezwodnika kwasowego.
Cykliczne bezwodniki
W przeciwieństwie do innych kwasów karboksylowych, które wymagają chlorku acylu, kwasy dikarboksylowe można kondensować w odpowiadającym im bezwodniku. W tym celu konieczne jest podgrzanie ich, aby promować uwalnianie H2O. Na przykład pokazano tworzenie bezwodnika ftalowego z kwasu ftalowego.

Zwróć uwagę, jak pierścień pięciokątny jest ukończony, a tlen, który wiąże obie grupy C = O, jest jego częścią; To cykliczny bezwodnik. Można również zauważyć, że bezwodnik ftalowy jest bezwodnikiem symetrycznym, ponieważ oba R1 jak R2 Są identyczne: pierścień aromatyczny.
Nie wszystkie kwasy dikarboksylowe są zdolne do tworzenia bezwodnika, ponieważ gdy ich grupy COOH są szeroko rozdzielone, są zmuszone do uzupełniania coraz większych pierścieni. Największym pierścieniem, który można uformować, jest pierścień sześciokątny, większy niż nie zachodzi reakcja.
Nomenklatura
Jak nazywa się bezwodniki? Pomijając nieorganiczne związki, związane z tlenkami, nazwy bezwodników organicznych dotychczas wyjaśnione zależą od tożsamości R1 i R2; to znaczy z jego grup acylowych.
Jeśli dwa R są takie same, wystarczy zastąpić słowo „acid” słowem „bezwodnik” w odpowiedniej nazwie kwasu karboksylowego. A jeśli, przeciwnie, dwa R są różne, są one nazwane w porządku alfabetycznym. Dlatego, aby wiedzieć, jak to nazwać, należy najpierw sprawdzić, czy jest to symetryczny lub asymetryczny bezwodnik kwasowy.
The (CH3CO)2Albo jest symetryczny, ponieważ R1= R2 = CH3. Pochodna kwasu octowego lub etanowego, a więc jego nazwa, zgodnie z poprzednim wyjaśnieniem: bezwodnik octowy lub etanowy. To samo dotyczy właśnie wspomnianego bezwodnika ftalowego.
Załóżmy, że masz następujący bezwodnik:
CH3CO (O) COCH2CH2CH2CH2CH2CH3
Grupa acetylowa po lewej pochodzi z kwasu octowego, a ta po prawej pochodzi z kwasu heptanowego. Aby nazwać ten bezwodnik, musisz nazwać swoje grupy R w kolejności alfabetycznej. Tak więc nazywa się: bezwodnik octowy heptanowy.
Aplikacje
Nieorganiczne bezwodniki mają nieskończoną liczbę zastosowań, od syntezy i formułowania materiałów, ceramiki, katalizatorów, cementów, elektrod, nawozów itp., Po powlekanie skorupy ziemskiej tysiącami minerałów żelaza i glinu oraz dwutlenku. węgla wydychanego przez żywe organizmy.
Stanowią one źródło wyjścia, punkt, w którym powstaje wiele związków stosowanych w syntezie nieorganicznej. Jednym z najważniejszych bezwodników jest dwutlenek węgla, CO2. Jest wraz z wodą niezbędny do fotosyntezy. A na poziomie przemysłowym SO3 to jest najważniejsze, ponieważ oskarżony otrzymuje z niego kwas siarkowy.
Być może bezwodnik o większej liczbie zastosowań i (o ile istnieje życie) jest jednym z kwasu fosforowego: trójfosforanu adenozyny, lepiej znanego jako ATP, obecnego w DNA i „walucie energetycznej” metabolizmu.
Bezwodniki organiczne
Bezwodniki kwasowe reagują przez acylowanie, albo na alkohol, tworząc ester, na aminę, powodując powstanie amidu, albo pierścienia aromatycznego.
Istnieją miliony każdego z tych związków i setki tysięcy opcji kwasu karboksylowego do przygotowania bezwodnika; dlatego możliwości syntetyczne rosną drastycznie.
Zatem jednym z głównych zastosowań jest włączenie grupy acylowej do związku, zastępując jeden z atomów lub grup jego struktury.
Każdy bezwodnik oddzielnie ma swoje własne zastosowania, ale ogólnie rzecz biorąc, wszystkie reagują w podobny sposób. Z tego powodu tego typu związki są wykorzystywane do modyfikowania struktur polimerowych, tworząc nowe polimery; to znaczy kopolimery, żywice, powłoki itp..
Na przykład bezwodnik octowy stosuje się do acetylowania wszystkich grup OH celulozy (dolny obraz). W ten sposób każde H z OH jest zastąpione grupą acetylową, COCH3.
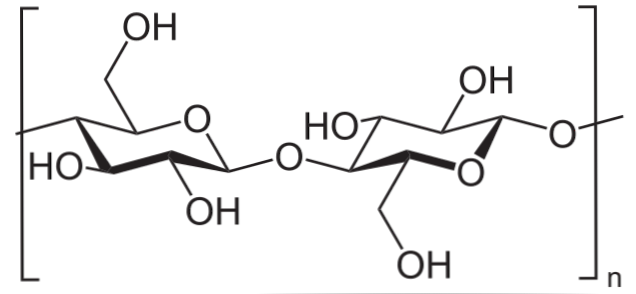
W ten sposób otrzymuje się polimer octanu celulozy. Ta sama reakcja może być nakreślona innymi strukturami polimerowymi z grupami NH2, również podatne na acylację.
Te reakcje acylowania są także użyteczne w syntezie leków, takich jak aspiryna (kwas acetylsalicylowy).
Przykłady
Pokazano, że niektóre inne przykłady bezwodników organicznych kończą się. Chociaż nie będzie o nich żadnej wzmianki, atomy tlenu można zastąpić siarką, siarką, a nawet bezwodnikami fosforu.
-C6H5CO (O) COC6H5: bezwodnik benzoesowy. Grupa C6H5 oznacza pierścień benzenowy. Jego hydroliza wytwarza dwa kwasy benzoesowe.
-HCO (O) COH: bezwodnik mrówkowy. Jego hydroliza wytwarza dwa kwasy mrówkowe.
- C6H5CO (O) COCH2CH3: benzoesowy bezwodnik propanowy. Jego hydroliza wytwarza kwasy benzoesowy i propanowy.
-C6H11CO (O) COC6H11: bezwodnik cykloheksanokarboksylowy. W przeciwieństwie do pierścieni aromatycznych są one nasycone, bez podwójnych wiązań.
-CH3CH2CH2CO (O) COCH2CH3: butanowy bezwodnik propanowy.
Bezwodnik bursztynowy

Mamy tu kolejny cykliczny, pochodzący z kwasu bursztynowego, kwas dikarboksylowy. Zauważ, jak trzy atomy tlenu zdradzają chemiczny charakter tego typu związku.
Bezwodnik maleinowy jest bardzo podobny do bezwodnika bursztynowego, z tą różnicą, że między węglami tworzącymi podstawę pięciokąta występuje podwójne wiązanie.
Bezwodnik glutarowy
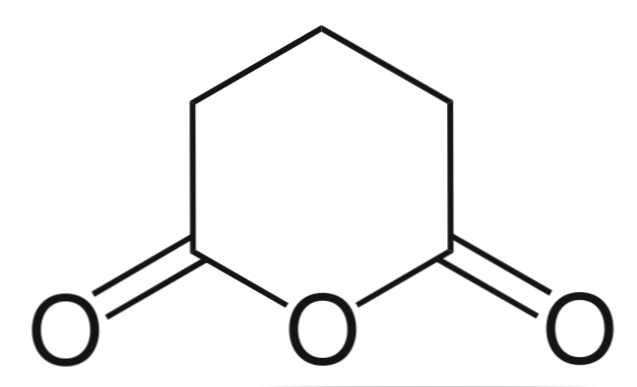
I wreszcie pokazano bezwodnik kwasu glutarowego. To strukturalnie odróżnia się od wszystkich innych składając się z sześciokątnego pierścienia. Ponownie, trzy atomy tlenu wyróżniają się w strukturze.
Inne bezwodniki, bardziej złożone, zawsze mogą być udowodnione przez trzy atomy tlenu bardzo blisko siebie.
Referencje
- Redakcja Encyclopaedia Britannica. (2019). Bezwodnik. Encryclopaedia Britannica. Źródło: britannica.com
- Helmenstine, Anne Marie, Ph.D. (8 stycznia 2019 r.). Definicja Acid Anhydride in Chemistry. Źródło: thinkco.com
- Chemia LibreTexts. (s.f.). Bezwodniki. Źródło: chem.libretexts.org
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chemia organiczna. Aminy (10th wydanie.). Wiley Plus.
- Carey F. (2008). Chemia organiczna (Szósta edycja). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Chemia (8 wyd.). CENGAGE Learning.
- Morrison i Boyd. (1987). Chemia organiczna (Piąta edycja). Addison-Wesley Iberoamericana.
- Wikipedia. (2019). Bezwodnik kwasu organicznego. Źródło: en.wikipedia.org


