Struktura, właściwości, nazewnictwo i zastosowania tlenku srebra (Ag2O)
The tlenek srebra jest związkiem nieorganicznym, którego wzór chemiczny to Ag2O. Siła, która jednoczy atomy, ma charakter całkowicie jonowy; dlatego składa się z jonowego ciała stałego, w którym występuje stosunek dwóch kationów Ag+ oddziaływanie elektrostatyczne z anionem O2-.
Anion tlenkowy, O2-, wynika to z interakcji srebrowych atomów powierzchni z tlenem środowiska; w bardzo podobny sposób do żelaza i wielu innych metali. Srebrny kawałek lub biżuteria zamiast zaczerwienienia i kruszenia się w rdzę, zmienia kolor na czarny, charakterystyczny dla tlenku srebra.

Na przykład na obrazku powyżej widać zardzewiały srebrny kubek. Zwróć uwagę na jego poczerniałą powierzchnię, chociaż wciąż zachowuje pewien dekoracyjny połysk; dlatego nawet zardzewiałe srebrne przedmioty można uznać za wystarczająco atrakcyjne dla celów dekoracyjnych.
Właściwości tlenku srebra są takie, że na pierwszy rzut oka nie psują oryginalnej metalicznej powierzchni. Powstaje w temperaturze pokojowej przez prosty kontakt z tlenem w powietrzu; a co jeszcze bardziej interesujące, może się rozkładać w wysokich temperaturach (powyżej 200 ° C).
Oznacza to, że jeśli szklanka obrazu zostałaby zatrzymana, a ciepło intensywnego płomienia zostało zastosowane, odzyskałoby srebrzysty połysk. Dlatego jego tworzenie jest procesem odwracalnym termodynamicznie.
Tlenek srebra ma również inne właściwości i, poza jego prostą formułą Ag2Lub obejmuje złożone organizacje strukturalne i bogatą różnorodność brył. Jednak Ag2Czy może jest to obok Ag2O3, najbardziej reprezentatywny z tlenków srebra.
Indeks
- 1 Struktura tlenku srebra
- 1.1 Zmiany z numerem Walencji
- 2 Właściwości fizyczne i chemiczne
- 2.1 Masa cząsteczkowa
- 2.2 Wygląd
- 2.3 Gęstość
- 2.4 Temperatura topnienia
- 2,5 Kps
- 2.6 Rozpuszczalność
- 2.7 Charakter kowalencyjny
- 2.8 Dekompozycja
- 3 Nazewnictwo
- 3.1 Walencja I i III
- 3.2 Systematyczne nazewnictwo złożonych tlenków srebra
- 4 zastosowania
- 5 referencji
Struktura tlenku srebra
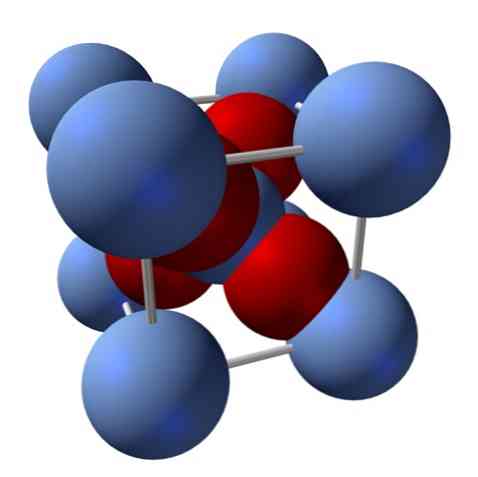
Jak wygląda jego struktura? Jak wspomniano na początku: jest to jonowe ciało stałe. Z tego powodu w strukturze nie mogą występować wiązania kowalencyjne Ag - O ani Ag = O; ponieważ gdyby tak było, właściwości tego tlenku zmieniłyby się drastycznie. To wtedy jony Ag+ i O2- w stosunku 2: 1 i doświadcza przyciągania elektrostatycznego.
Strukturę tlenku srebra określa w konsekwencji sposób, w jaki siły jonowe wyrzucają w przestrzeń jony Ag+ i O2-.
Na przykład na górnym obrazie znajduje się komórka elementarna dla sześciennego układu krystalicznego: kationy Ag+ są srebrne niebieskie kule i O2- czerwonawe kule.
Jeśli policzysz liczbę kulek, przekonasz się, że na pierwszy rzut oka jest dziewięć srebrno-niebieskich i cztery czerwone kolory. Jednak tylko fragmenty sfer zawartych w sześcianie są brane pod uwagę; licząc je, będące ułamkami całkowitych kulek, stosunek Ag: 2: 1 musi być spełniony2O.
Powtarzanie jednostki strukturalnej czworościanu AgO4 otoczony czterema innymi Ag+, cała czarna bryła jest zbudowana (eliminując luki lub nieprawidłowości, które mogą mieć te układy kryształów).
Zmiany z numerem Walencji
Skupiając się teraz nie na czworościanie AgO4 ale w linii AgOAg (obserwuj wierzchołki górnego sześcianu) będzie to, że stały tlenek srebra składa się z innej perspektywy wielu warstw jonowych ułożonych liniowo (choć nachylonych). Wszystko to w wyniku „molekularnej” geometrii wokół Ag+.
Powyższe zostało potwierdzone przez kilka badań nad jego strukturą jonową.
Srebro działa głównie z wartościowością +1, ponieważ w przypadku utraty elektronu jego wynikowa konfiguracja elektronowa to [Kr] 4d10, który jest bardzo stabilny. Inne wartościowości, takie jak Ag2+ i Ag3+ są mniej stabilne, ponieważ tracą elektrony z orbitali prawie całkowicie wypełnione.
Jon Ag3+, jest jednak mniej niestabilny w porównaniu z Ag2+. W rzeczywistości może współistnieć w firmie Ag+ Chemicznie wzbogaca strukturę.
Jego konfiguracja elektroniczna to [Kr] 4d8, z niesparowanymi elektronami w taki sposób, który daje mu pewną stabilność.
W przeciwieństwie do geometrii liniowych wokół jonów Ag+, stwierdzono, że jony Ag3+ Jest kwadratowy płaski. Dlatego tlenek srebra z jonami Ag3+ składałby się z warstw złożonych z kwadratów AgO4 (nie czworościany) połączone elektrostatycznie liniami AgOAg; Tak jest w przypadku Ag4O4 Ag2O ∙ Ag2O3 ze strukturą jednoskośną.
Właściwości fizyczne i chemiczne

Jeśli zarysujesz powierzchnię srebrnego kubka głównego obrazu, otrzymasz bryłę, która jest nie tylko czarna, ale ma również brązowe lub brązowe odcienie (górny obraz). Niektóre z jego właściwości fizycznych i chemicznych zgłaszane przez te momenty są następujące:
Masa cząsteczkowa
231,735 g / mol
Wygląd
Jednolity czarny brąz w postaci proszku (należy zauważyć, że mimo że jest ciałem stałym, nie ma krystalicznego wyglądu). Jest bezwonny i zmieszany z wodą nadaje metaliczny smak
Gęstość
7,14 g / ml.
Temperatura topnienia
277-300 ° C Z pewnością rozpływa się w stałe srebro; to znaczy prawdopodobnie rozpada się przed utworzeniem ciekłego tlenku.
Kps
1,52 ∙ 10-8 w wodzie o temperaturze 20 ° C Jest zatem związkiem słabo rozpuszczalnym w wodzie.
Rozpuszczalność
Jeśli przyjrzysz się uważnie obrazowi jego struktury, przekonasz się, że kule Ag2+ i O2- Nie zgadzają się prawie pod względem wielkości. W rezultacie tylko małe cząsteczki mogą przenikać do wnętrza sieci krystalicznej, czyniąc ją nierozpuszczalną w prawie wszystkich rozpuszczalnikach; z wyjątkiem tych, w których reaguje, takich jak zasady i kwasy.
Kowalencyjny charakter
Chociaż wielokrotnie powtarzano, że tlenek srebra jest związkiem jonowym, pewne właściwości, takie jak jego niska temperatura topnienia, przeczą temu stwierdzeniu.
Z pewnością uwzględnienie charakteru kowalencyjnego nie rozbija tego, co wyjaśniono dla jego struktury, wystarczyłoby dodać go do struktury Ag2Lub model sfer i prętów wskazujących wiązania kowalencyjne.
Również czworościany i płaszczyzny kwadratowe AgO4, podobnie jak linie AgOAg, byłyby one połączone wiązaniami kowalencyjnymi (lub kowalencyjnymi jonowymi).
Mając to na uwadze, Ag2Albo w rzeczywistości byłby to polimer. Zaleca się jednak, aby uznać ją za ciało jonowe o charakterze kowalencyjnym (którego charakter połączenia jest wciąż wyzwaniem).
Rozkład
Początkowo wspomniano, że jego tworzenie jest termodynamicznie odwracalne, więc pochłania ciepło, aby powrócić do stanu metalicznego. Wszystko to można wyrazić za pomocą dwóch równań chemicznych dla takich reakcji:
4Ag (s) + O2(g) => 2Ag2O (s) + Q
2Ag2O (s) + Q => 4Ag (s) + O2(g)
Gdzie Q reprezentuje ciepło w równaniu. To wyjaśnia, dlaczego ogień płonący na powierzchni zardzewiałej srebrnej filiżanki przywraca jej srebrzysty połysk.
Dlatego trudno założyć, że istnieje Ag2O (l), ponieważ natychmiast rozkładałby się pod wpływem ciepła; chyba że ciśnienie jest zbyt wysokie, aby uzyskać wspomnianą brązową czarną ciecz.
Nomenklatura
Gdy wprowadzono możliwość jonów Ag2+ i Ag3+ oprócz wspólnego i dominującego Ag+, określenie „tlenek srebra” zaczyna wydawać się niewystarczające, aby odnieść się do Ag2O.
To dlatego, że jon Ag+ jest bardziej obfity niż inne, więc Ag jest brany2Lub jako jedyny tlenek; co nie jest w ogóle poprawne.
Jeśli myślisz o Ag2+ ponieważ praktycznie nie istnieje, biorąc pod uwagę jego niestabilność, wtedy tylko jony o wartościowości +1 i +3 będą obecne; to znaczy Ag (I) i Ag (III).
Walencja I i III
Będąc najmniejszą wartościowością Ag (I), nazywa się ją przez dodanie przyrostka -oso do jej nazwy argentum. Więc Ag2Lub jest to: tlenek argentozo lub, zgodnie z nomenklaturą systematyczną, tlenek dyplomatyczny.
Jeśli Ag (III) jest całkowicie ignorowany, to jego tradycyjna nomenklatura musi być: tlenkiem srebra zamiast tlenkiem argentyńskim.
Z drugiej strony, Ag (III) będący większą wartościowością dodaje przyrostek -ico do swojej nazwy. Więc Ag2O3 jest: tlenek srebra (jony 2 Ag)3+ z trzema O2-). Również jego nazwa zgodna z systematyczną nomenklaturą brzmiałaby: trójtlenek dyplomy.
Jeśli obserwuje się strukturę Ag2O3, można przypuszczać, że jest to produkt utleniania przez ozon, OR3, zamiast tlenu. Dlatego jego kowalencyjny charakter musi być większy, ponieważ jest to związek kowalencyjny z wiązaniami Ag-O-O-O-Ag lub Ag-O.3-Ag.
Systematyczne nazewnictwo złożonych tlenków srebra
AgO, również napisany jako Ag4O4 Ag2O ∙ Ag2O3, jest to tlenek srebra (I, III), ponieważ ma zarówno wartościowości +1, jak i +3. Jego nazwa zgodna z systematyczną nomenklaturą brzmiałaby: czterotlenek tetraplatu.
Ta nomenklatura jest bardzo pomocna, jeśli chodzi o inne stechiometrycznie bardziej złożone tlenki srebra. Załóżmy na przykład, że dwie bryły 2Ag2O ∙ Ag2O3 i Ag2O ∙ 3Ag2O3.
Pisanie pierwszego w bardziej odpowiedni sposób to: Ag6O5 (liczenie i dodawanie atomów Ag i O). Nazywałby się wtedy pięciotlenkiem heksaplatu. Należy zauważyć, że ten tlenek ma mniejszą zawartość srebra niż Ag2O (6: 5 < 2:1).
Podczas pisania drugiej bryły w przeciwnym razie byłoby to: Ag8O10. Jego nazwa to dekanolan oktaplatu (o stosunku 8:10 lub 4: 5). Ten hipotetyczny tlenek srebra byłby „bardzo utleniony”.
Używa
Badania nad poszukiwaniem nowych i zaawansowanych zastosowań tlenku srebra są nadal prowadzone. Niektóre z jego zastosowań są wymienione poniżej:
-Rozpuszcza się w amoniaku, azotanie amonu i wodzie, tworząc odczynnik Tollensa. Odczynnik ten jest przydatnym narzędziem w analizach jakościowych w laboratoriach chemii organicznej. Pozwala określić obecność aldehydów w próbce, pozytywną odpowiedzią jest utworzenie „srebrnego lustra” w probówce.
-Wraz z cynkiem metalicznym tworzy podstawowe baterie tlenku cynku srebra. Jest to prawdopodobnie jedno z jego najbardziej popularnych i domowych zastosowań.
-Służy jako oczyszczacz gazu, pochłaniając na przykład CO2. Po ogrzaniu uwalnia uwięzione gazy i może być ponownie użyty kilka razy.
-Ze względu na przeciwdrobnoustrojowe właściwości srebra jego tlenek jest przydatny w badaniach bioanalizy i oczyszczania gleby.
-Jest to łagodny środek utleniający zdolny do utleniania aldehydów do kwasów karboksylowych. Jest także stosowany w reakcji Hofmanna (aminy trzeciorzędowe) i bierze udział w innych reakcjach organicznych, zarówno jako odczynnik, jak i katalizator.
Referencje
- Bergstresser M. (2018). Tlenek srebra: Formuła, rozkład i tworzenie. Studiować Źródło: study.com
- Autorzy i redaktorzy tomów III / 17E-17F-41C. (s.f.). Tlenki srebra (Ag (x) O (y)) struktura krystaliczna, parametry sieci. (Dane liczbowe i zależności funkcjonalne w nauce i technologii), tom 41C. Springer, Berlin, Heidelberg.
- Mahendra Kumar Trivedi, Rama Mohan Tallapragada, Alice Branton, Dahryn Trivedi, Gopal Nayak, Omprakash Latiyal, Snehasis Jana. (2015). Potencjalny wpływ oczyszczania energii z biopola na właściwości fizyczne i termiczne proszku tlenku srebra. International Journal of Biomedical Science and Engineering. Vol. 3, No. 5, pp. 62-68. doi: 10.11648 / j.ijbse.20150305.11
- Sullivan R. (2012). Rozkład tlenku srebra. University of Oregon Źródło: chemdemos.uoregon.edu
- Flint, Deyanda. (24 kwietnia 2014 r.). Zastosowania baterii z tlenkiem srebra. Nauka. Źródło: sciencing.com
- Salman Montasir E. (2016). Badanie niektórych właściwości optycznych tlenku srebra (Ag2o) przy użyciu spektrofotometru UVVisible. [PDF] Źródło: iosrjournals.org
- Bard Allen J. (1985). Standardowe potencjały w wodnym roztworze. Marcel Dekker. Źródło: books.google.co.ve


