Saponification Reaction and Substances, które można uzyskać
The zmydlanie Jest to podstawowa hydroliza estru. Oznacza to, że ester reaguje z zasadą (NaOH lub KOH) nieodwracalnie, wytwarzając alkohol i karboksylany sodu lub potasu. Słowo to oznacza „wytwarzanie mydeł” i jest jedną z najstarszych reakcji chemicznych stosowanych przez ludzkość.
W czasach babilońskich, z pomocą popiołów zebranych z drewna, roślin i tłuszczów zwierzęcych, udoskonalili sztukę wytwarzania mydeł. Dlaczego tłuszcz zwierzęcy? Powodem jest to, że jest bogaty w triestry glicerolu (triglicerydy), a popioły drzewne są źródłem potasu, podstawowego metalu.
W przeciwnym razie reakcja przebiega z mniejszą wydajnością, ale wystarczająco, aby odzwierciedlić jej wpływ na farby i niektóre powierzchnie. Tak jest w przypadku obrazów olejnych, gdzie pigmenty miesza się z olejem (źródło estrów).
Indeks
- 1 Reakcja zmydlania
- 1.1 Mechanizm
- 1.2 Kinetyka
- 2 Substancje, które można uzyskać przez zmydlanie
- 2.1 Działanie rozpuszczalników mydeł
- 3 referencje
Reakcja zmydlania
Mechanizm
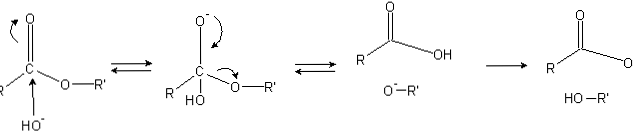
Estry mają grupę acylową (O = C-R), która jest podatna na ataki nukleofilowe, takie jak OH-.
Ponieważ atomy tlenu „kradną” gęstość elektronową z atomu węgla, jest on częściowo naładowany, tym bardziej w przypadku estrów.
W konsekwencji ten ładunek dodatni przyciąga negatywne gatunki zdolne do dostarczania elektronów do atomu węgla, z atakiem nukleofilowym (po lewej stronie obrazu). W rezultacie powstaje tetraedryczny produkt pośredni (druga cząsteczka od lewej do prawej).
Ujemny ładunek tlenu w tetraedrycznym półprodukcie jest produktem OH- otoczenie Następnie ten ładunek ujemny jest delokalizowany, aby zapoczątkować grupę karbonylową, „zmuszając”, a następnie do rozbicia wiązania C-OR ”. Również to przeniesienie wytwarza kwas karboksylowy RCOOH i jon alkoholanowy R'O-.
Wreszcie, gdy środowisko reakcji jest zasadowe, alkoholan deprotonuje jedną cząsteczkę wody, a kwas karboksylowy reaguje z innym OH- medium, wytwarzając produkty zmydlania.
Kinetyka
Szybkość reakcji zmydlania jest proporcjonalna do stężeń reagentów. Innymi słowy, zwiększenie stężenia estru (RCOOR ') lub zasady (NaOH), reakcja będzie przebiegać z większą szybkością.
Jest to również tłumaczone w następujący sposób: szybkość zmydlania jest pierwszym rzędem w odniesieniu do estru i pierwszym rzędem w odniesieniu do podstawy. Powyższe można wyrazić za pomocą następującego równania matematycznego:
Speed = k [RCOOR ”] [NaOH]
Gdzie k jest stałym lub współczynnikiem prędkości, który zmienia się w funkcji temperatury lub ciśnienia; to znaczy, im wyższe ciepło, tym większa prędkość zmydlania. Z tego powodu medium jest wrzące.
Ponieważ oba odczynniki mają kinetykę pierwszego rzędu, ogólna reakcja jest drugą kolejnością.
W mechanizmie reakcji zmydlania, tworzenie tetraedrycznego związku pośredniego wymaga ataku nukleofilowego, który obejmuje zarówno ester, jak i zasadę.
Tak więc kinetyka drugiego rzędu znajduje odzwierciedlenie w tym fakcie, ponieważ interweniują w (powolnym) etapie determinant reakcji.
Substancje, które można uzyskać przez zmydlanie

Głównymi produktami zmydlania są alkohole i sole kwasów karboksylowych. W środowisku kwaśnym otrzymuje się odpowiedni RCOOH, otrzymany przez zmydlanie tłuszczów i olejów, znanych jako kwasy tłuszczowe..
W ten sposób mydła składają się z soli kwasów tłuszczowych powstałych w wyniku zmydlania. Czy wychodzisz z jakim kationem? Mogą być Na+, K+, Mg2+, Wiara3+, itd..
Sole te są rozpuszczalne w wodzie, ale wytrącają się w wyniku działania NaCl dodanego do mieszaniny, która odwadnia mydło i oddziela je od fazy wodnej. Reakcja zmydlania triglicerydu jest następująca:
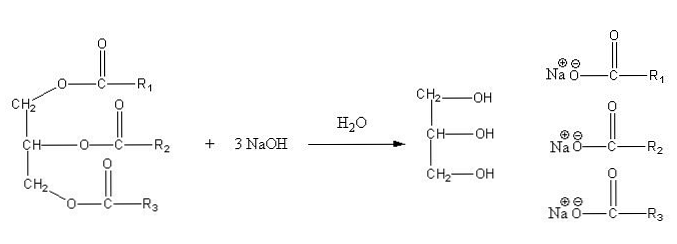
Gliceryna jest alkoholowym „E”, a mydło to wszystkie sole otrzymanych kwasów tłuszczowych. Tutaj każdy łańcuch boczny -R ma różne długości i stopień nienasycenia. W konsekwencji łańcuchy te stanowią różnicę między tłuszczami i olejami roślinnymi.
Kluczem do produkcji mydeł jest wybór najlepszych tłuszczów i olejów, a dokładniej wybór różnych źródeł triglicerydów.
Ta biała masa mydlana może zawierać barwniki i inne związki organiczne w swojej strukturze, nadając jej przyjemny aromat i jasne kolory. Stąd zakres możliwości jest oswojony przez sztukę i powołanie w tej branży.
Jednak reakcja zmydlania jest również syntetyczną drogą kwasów karboksylowych i alkoholi, które niekoniecznie muszą mieć związek z gliceryną lub mydłami.
Na przykład, podstawowa hydroliza dowolnego estru, takiego jak prosty octan etylu, wytworzy kwas octowy i etanol.
Rozpuszczalnikowe działanie mydeł

Sole kwasów tłuszczowych są rozpuszczalne w wodzie, ale nie w taki sam sposób jak solwatowane jony; to znaczy otoczona wodną kulą. W przypadku mydeł ich łańcuchy boczne -R teoretycznie uniemożliwiają ich rozpuszczenie w wodzie.
Dlatego, aby przeciwdziałać tej niewygodnej energetycznie pozycji, są one zorientowane w taki sposób, że łańcuchy wchodzą w kontakt, tworząc apolarne jądro organiczne, podczas gdy głowy polarne, koniec (-COO)- Na+), oddziaływać z cząsteczkami wody i tworzyć „skorupę polarną”.
Powyższe zilustrowano na powyższym obrazku, na którym pokazano ten typ struktury znany jako micela.
„Czarne ogony” odpowiadają hydrofobowym łańcuchom, zaplątanym w organiczny rdzeń chroniony przez szare kule. Te szare kule tworzą tarczę polarną, głowy -COO- Na+.
Następnie micele są skupiskami (skupiskami) soli kwasów tłuszczowych. W nich mogą otaczać tłuszcz, który jest nierozpuszczalny w wodzie ze względu na jego niepolarny charakter.
Jak oni to robią? Zarówno łańcuch tłuszczowy, jak i łańcuch -R są hydrofobowe, więc oba mają duże powinowactwo do siebie nawzajem.
Gdy micele otaczają tłuszcze, woda oddziałuje z otoczką polarną, umożliwiając rozpuszczalność mydła. Podobnie micele są naładowane ujemnie, powodując wzajemne odpychanie, a zatem wytwarzając dyspersję tłuszczu.
Referencje
- Anne Marie Helmenstine, Ph.D. (3 października 2017). Definicja zmydlania i reakcja. Źródło: 24 kwietnia 2018 r. Z: thoughtco.com
- Francis A. Carey. Chemia organiczna Kwasy karboksylowe. (wydanie szóste., str. 863-866). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. Chemia organiczna. Lipidy (wydanie 10., strona 1056-1058). Wiley Plus.
- Wikipedia. (2018). Zmydlanie. Źródło: 24 kwietnia 2018 r. Z: en.wikipedia.org
- Boyd C. (27 lutego 2015). Zrozum chemię i historię mydła. Źródło: 24 kwietnia 2018, z: chemservice.com
- Luca Laghi (27 marca 2007). Zmydlanie. Źródło: 24 kwietnia 2018 r. Z: commons.wikimedia.org
- Amanda Crochet (12 maja 2015). Micelle (skala szarości). Źródło: 24 kwietnia 2018 r. Z: commons.wikimedia.org


