Proces reakcji egzotermicznej, typy i przykłady
The reakcja egzotermiczna jest rodzajem reakcji chemicznej, w której następuje transfer energii, głównie w postaci uwalniania ciepła lub światła. Nazwa pochodzi od greckiego przedrostka exo, co oznacza „za granicą”; i termin „termiczny”, który odnosi się do ciepła lub temperatury.
W tym sensie reakcje egzotermiczne mogą przenosić inne rodzaje energii do środowiska, w którym są wytwarzane, takie jak eksplozje i ich sposób przenoszenia energii kinetycznej i dźwiękowej, gdy substancje znajdujące się w fazie gazowej w wysokich temperaturach są rozszerzane. gwałtowny sposób.
W ten sam sposób, w przypadku użycia baterii, przeprowadzana jest również reakcja egzotermiczna, tylko w tym przypadku energia elektryczna jest transportowana.
Indeks
- 1 Proces
- 2 typy
- 2.1 Reakcje spalania
- 2.2 Reakcje neutralizacji
- 2.3 Reakcje utleniania
- 2.4 Reakcja termitowa
- 2.5 Polimeryzacja reakcji
- 2.6 Reakcja rozszczepienia jądrowego
- 2.7 Inne reakcje
- 3 Przykłady
- 4 odniesienia
Proces
Poprzednio wspominano, że gdy zachodzi reakcja egzotermiczna, następuje uwolnienie energii, które można łatwiej zwizualizować w następującym równaniu:
Odczynniki (s) → Produkt (y) + Energia
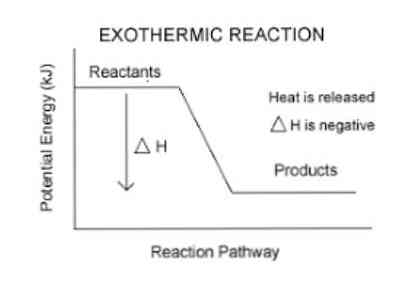
Tak więc, aby określić ilość energii pochłoniętej lub uwolnionej przez układ, stosuje się parametr termodynamiczny o nazwie entalpia (oznaczony jako „H”). Jeśli w systemie (w tym przypadku jest to reakcja chemiczna) następuje uwolnienie energii do otoczenia, wówczas zmiana entalpii (wyrażona jako ΔH) będzie miała wartość ujemną.
W przeciwnym razie, jeśli zmiana tego środka jest dodatnia, odzwierciedla absorpcję ciepła z otoczenia. Ponadto wielkość zmienności entalpii systemu jest wyrazem ilości energii, która jest przenoszona do lub ze środowiska.
Im większa wartość ΔH, tym większe uwalnianie energii z systemu do otaczającego medium.
Dzieje się tak, ponieważ w tych reakcjach energia netto, która jest uwalniana, gdy tworzone są nowe połączenia, jest większa niż energia netto wykorzystana do fragmentacji łączy.
Z powyższego można wywnioskować, że ten rodzaj reakcji jest bardzo powszechny, ponieważ produkty reakcji mają pewną ilość energii zmagazynowanej w wiązaniach, która jest większa niż ilość zawarta w reagentach..
Typy
Istnieją różne rodzaje reakcji egzotermicznych w różnych dziedzinach chemii, zarówno w laboratorium, jak iw przemyśle; niektóre są przeprowadzane spontanicznie, a inne wymagają specyficznych warunków lub jakiegoś rodzaju substancji, takiej jak katalizator.
Oto najważniejsze rodzaje reakcji egzotermicznych:
Reakcje spalania
Reakcje spalania to reakcje typu redoks, które zachodzą, gdy jedna lub więcej substancji reaguje z tlenem, generalnie powodując uwolnienie światła i energii cieplnej, czyli światło i ciepło, gdy powstaje płomień..
Reakcje neutralizacji
Reakcje neutralizacji charakteryzują się interakcją między kwasem a substancją alkaliczną (zasadą) z wytworzeniem soli i wody, które wykazują egzotermiczny charakter.
Reakcje utleniania
Istnieje wiele reakcji tego typu, które wykazują zachowanie egzotermiczne, ponieważ utlenianie tlenu powoduje uwalnianie dużej ilości energii, co zachodzi podczas utleniania węglowodorów..
Reakcja termitów
Ta reakcja może wytworzyć temperaturę w przybliżeniu 3000 ° C, a ze względu na wysokie powinowactwo proszku aluminiowego do dużej liczby tlenków metali, jest ono wykorzystywane do spawania stali i żelaza.
Reakcja polimeryzacji
Ten typ reakcji powstaje, gdy reaguje pewna liczba związków chemicznych zwanych monomerami, które są jednostkami, które po połączeniu powtarzają się w łańcuchach, tworząc struktury makrocząsteczkowe zwane polimerami.
Reakcja rozszczepienia jądrowego
Proces ten odnosi się do podziału jądra atomu uważanego za ciężki - to znaczy o liczbie masowej (A) większej niż 200 - w celu wytworzenia fragmentów lub jąder o mniejszym rozmiarze z masą pośrednią.
W tej reakcji, w której powstaje jeden lub więcej neutronów, uwalniana jest duża ilość energii, ponieważ rdzeń o większej masie ma niższą stabilność niż jego produkty.
Inne reakcje
Istnieją także inne reakcje egzotermiczne o dużym znaczeniu, takie jak odwodnienie niektórych węglowodanów podczas reakcji z kwasem siarkowym, absorpcja wody zawierającej wodorotlenek sodu wystawiony na działanie powietrza lub utlenianie związków metali w wielu reakcjach korozyjnych.
Przykłady
Poniżej znajdują się przykłady reakcji egzotermicznych, które powodują zmianę entalpii, która ma wartość ujemną, ponieważ uwalniają energię, jak wspomniano powyżej..
Na przykład spalanie propanu jest spontaniczną reakcją egzotermiczną:
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O (l)
Inny przypadek zachowania egzotermicznego wynika z reakcji neutralizacji pomiędzy węglanem sodu i kwasem chlorowodorowym:
NaHCO3(ac) + HCl (ac) → NaCl (ac) + H2O (l) + CO2(g)
Przedstawiono także utlenianie etanolu do kwasu octowego stosowanego w alkomatach, którego pełną reakcję przedstawiono w następującym równaniu:
3CH3CH2OH + 2K2Cr2O7 + 8H2TAK4 → CH3COOH + 2Cr (SO4)3 + 2K2TAK4 + 11H2O
Inną klasą reakcji egzotermicznej jest tak zwana reakcja termitowa, w której aluminium łączy się z tlenkiem metalu, jak podano poniżej:
2Al (s) + Wiara2O3(s) → Al2O3(s) + Fe (l)
Oprócz przykładów wyjaśnionych powyżej, istnieje wiele różnych reakcji, które są również uważane za egzotermiczne, takie jak rozkład niektórych organicznych substancji odpadowych do kompostowania..
Podkreśla również utlenianie pigmentu lucyferyny przez działanie enzymu lucyferazy w celu wytworzenia bioluminescencji charakterystycznej dla świetlików, a nawet oddychania, wśród wielu innych reakcji.
Referencje
- Wikipedia. (s.f.). Reakcja egzotermiczna. Pobrane z es.wikipedia.org
- BBC (s.f.). Zmiany energii i reakcje odwracalne. Pobrane z bbc.co.uk
- Chang, R. (2007). Chemia, dziewiąta edycja. (McGraw-Hill).
- Walker, D. (2007). Reakcje chemiczne. Pobrane z books.google.co.ve
- Saunders, N. (2007). Poznawanie reakcji chemicznych. Pobrane z books.google.co.ve


